Zika virus: mecanismo para una herencia precoz
La reciente epidemia a raíz del virus Zika (ZIKV) en América Latina coincidió con un aumento marcado de casos de microcefalia en recién nacidos. Sin embargo, la relación de causalidad entre la infección materna y las malformaciones cerebrales no se ha establecido firmemente. Recientes investigaciones muestran que existe una transmisión vertical del ZIKV en ratones, lo que provoca un deterioro en el desarrollo cerebral del feto. Mediante la inyección intraperitoneal de una cepa de ZIKV en estos roedores se estableció una infección de las células de la zona dorsal del ventrículo cerebral de los fetos, y de otros tipos celulares como las progenitoras neurales primarias, responsables del desarrollo de la corteza. En base a estos hallazgos es posible sugerir que la transmisión vertical de ZIKV afecta el desarrollo del cerebro y por otro lado, dan a conocer un valioso modelo de estudio para determinar mecanísticamente cómo actúa el virus, posibilitando la evaluación de estrategias terapéuticas y preventivas.
Patogénesis viral
Hasta hace poco, existían escasos estudios acerca del virus Zika (ZIKV), un flavivirus de ARN, hasta que en el año pasado grandes epidemias en las Américas se vieron acompañadas por manifestaciones clínicas inesperadamente severas. La infección en embarazadas ha emergido como una fuente de gran preocupación mundial, debido a su vinculación con anomalías congénitas, incluyendo microcefalia, aborto espontáneo y restricción del crecimiento intrauterino. Además, la infección por ZIKV en otros grupos etarios se ha asociado con trastornos neurológicos severos y con el síndrome de Guillain-Barré.
Los ciclos de transmisión entre humanos y los mosquitos Aedes aegypti en zonas urbanas puede causar grandes epidemias por el virus. Aunque los mosquitos son claramente la causa primaria de los brotes, otros modos, como la transmisión sexual, también han sido reportados. Hasta la fecha, todos los casos por vía sexual han sido desde hombres infectados hacia sus parejas. Por otro lado, también se ha descrito la persistencia viral en los testículos y en el esperma, sin embargo la "ventana" de la transmisión sexual sigue siendo incierta, lo que ha incrementado la aprehensión sobre el ciclo replicativo del ZIKV durante el embarazo.
El asunto acerca de la transmisión en el útero ha alcanzado tanta prominencia como la misma aparición de ZIKV en Brasil así como también en otras partes de América Latina. El motivo, es porque el brote se ha asociado con un aumento en el número de casos de microcefalia. Los datos que apoyan la transmisión vertical, y un rol causal para el ZIKV en el desarrollo de malformaciones congénitas incluyen la detección del ARN o antígenos virales en el líquido amniótico, placenta, o en tejidos cerebrales en fetos o recién nacidos, en quienes se diagnostica microcefalia después de la muerte en el útero o poco después del nacimiento. Además, un estudio prospectivo en embarazadas que han sido infectadas con ZIKV en Brasil, mostró que un 29% de los fetos presentaron anomalías gestacionales incluyendo microcefalia y un crecimiento intrauterino restringido, observándose además que en un subgrupo de estos casos ocurrió muerte fetal. Tomando en cuenta tal evidencia, se considera que el desarrollo de un modelo animal in utero para estudiar la transmisión e infección de ZIKV es de gran relevancia para establecer la causalidad, satisfacer criterios de pruebas de teratogenicidad, y para proporcionar un medio para la selección de candidatos vacunales y agentes terapéuticos.
A la fecha, cuatro estudios utilizando modelos de ratón han sido publicados recientemente, abordando la relación causal entre la infección por ZIKV durante el embarazo y cambios patológicos en los fetos. Tres de estos estudios introdujeron diferentes cepas de ZIKV en ratones hembra preñadas a través de vías de inoculación periférica (intravenosa, intraperitoneal, o subcutánea), y dos estudios inocularon directamente el virus en el cerebro fetal. Todos las investigaciones establecieron que la infección provoca un deterioro de células del sistema nervioso central y un estudio demostró la base celular de la transmisión de ZIKV desde la sangre materna al feto.
Los Flavivirus deben superar las defensas promovidas por la señalización celular mediada por el receptor del interferon de tipo I (IFN-I) con el fin de replicarse en las células del hospedero. En parte, el ZIKV logra esto mediante la inducción de la degradación de la molécula de señalización STAT2 (una proteína mensajera que se encuentra río abajo del receptor de IFN) en las células humanas. Debido a que ZIKV promueve una ineficiente degradación de stat2 en ratones, Jonathan J. Miner y colegas (Cell. 2016 May 19;165(5):1081-91) utilizaron estos animales deficientes en la señalización celular promovida por el receptor de IFN-1, de manera de lograr una alta viremia para que el virus alcance la placenta. Este grupo inoculó una cepa asiática contemporánea de ZIKV en la piel de los ratones hembra preñadas a tiempos tempranos de su gestación (equivalente al primer trimestre de embarazo en humanos) y se observó infección, lesiones e insuficiencia placentaria, además de una alta tasa de reabsorción fetal, lesión cerebral fetal y muerte de células neuronales. Estas observaciones recapitulan los resultados en seres humanos, los que se producen en algunas mujeres infectadas durante el primer y segundo trimestre del embarazo.
Además, este grupo identificó ARN y partículas virales dentro de trofoblastos fetales y de células endoteliales de la placenta, resultados que son consistentes con un tropismo por las células que recubren la interfaz materna - fetal y una ruta de infección transplacentaria (figura 1).
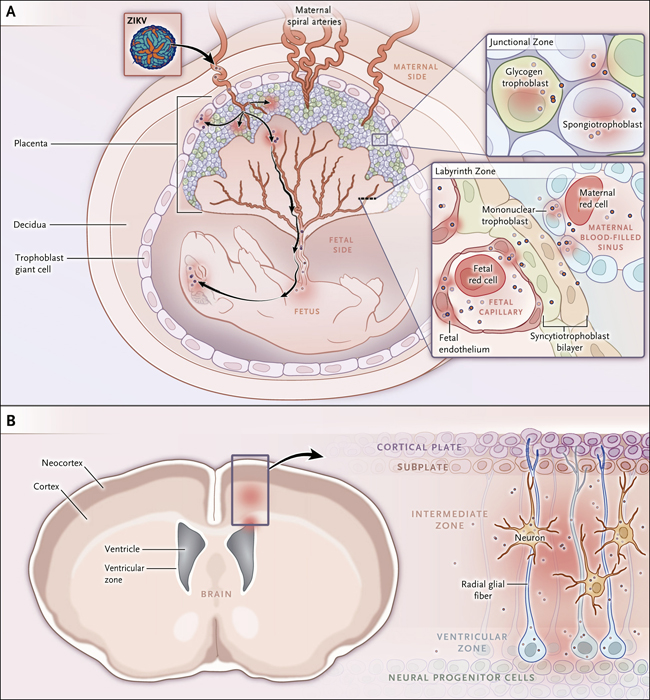
Figura 1. Sitios celulares de la infección por virus Zika (ZIKV) durante el embarazo.
La placenta de ratón comprende componentes maternos y fetales, incluyendo las zonas de unión y de laberinto (panel A). El ZIKV puede infectar a los trofoblastos placentarios, incluyendo diversos tipos, presentes en la zona de unión, además de trofoblastos mononucleares, sinusoides maternos, y células endoteliales que recubren los capilares fetales fetales en zona del laberinto. El virus infecta el cerebro fetal de ratón con tropismo por las células de la corteza cerebral y la zona ventricular, incluyendo células progenitoras neurales corticales y células gliales radiales (panel B). La infección conduce a una reducción de las capas corticales y de la cavidad ventricular debido a la muerte de células progenitoras neuronales y a la alteración de sus procesos, especialmente en zonas intermedias y ventriculares.
En otro estudio Fernanda R. Cugola y su equipo (Nature. 2016 May 11;534(7606):267-71) inocularon vía intravenosa a ratones SJL inmunocompetentes con una dosis extraordinariamente elevada (10e10-12 unidades formadoras de placas) con una cepa brasileña de ZIKV. Posiblemente, esta dosis permitió a algunas de los inóculos virales expandirse y alcanzar la placenta directamente sin requerir muchas fases replicativas en órganos periféricos, en donde se esperaría que sean inhibidos por IFN-I. Al igual que en las conclusiones de Miner y sus colegas, se observó una restricción del crecimiento intrauterino lo que resultó en crías más pequeñas al nacimiento. El examen de cerebros fetales y neonatales puso de manifiesto una disminución del número de neuronas corticales y del espesor de la capa cortical (figura 1). Los análisis celulares mostraron que las neuronas en la corteza cerebral, en el tálamo y en el hipotálamo habían sufrido deterioro. Además, se observaron anomalías oculares que eran similares a las que se han descrito en humanos (JAMA Ophthalmol. 2016;134(5):529-535).
Cui Li y colegas (Cell Stem Cell. 2016 Jul 7;19(1):120-6) y por otro lado el equipo liderado por Kong-Yan Wu (Cell Res. 2016 Jun;26(6):645-54) inyectaron cepas asiáticas contemporáneas de ZIKV directamente en el ventrículo lateral izquierdo del cerebro fetal en la fase gestacional E13.5 (equivalente al final del segundo trimestre de embarazo en humanos) y analizaron los tejidos antes y después del nacimiento. Ambos grupos observaron una reducción en el número de progenitores neurales corticales en zonas dorsales ventriculares y subventriculares, pérdida asociada con la muerte celular. Wu y sus colegas, además inyectaron ZIKV a través de una vía intraperitoneal en ratones hembra preñadas inmunocompetentes en la misma fase gestacional. Encontraron que el virus puede causar uns virema transitoria con orientación hacia la placenta en un subgrupo de estos animales. Además, inesperadamente, detectaron ARN viral en el ventrículo dorsal del cerebro fetal, pero no así en otras regiones del cerebro. Esto les permitió llegar a la conclusión de que ZIKV puede atravesar la barrera fetal - placentaria y dirigirse específicamente a progenitores neurales corticales de ratones en desarrollo.
Estos estudios sugieren que ZIKV accede al feto durante el embarazo después de cruzar la barrera placentaria, la que se compone de diferentes tipos de trofoblastos y células auxiliares (figura 1). Basándose en los modelos de estudio en ratones así como en los estudios recientes sobre infección en células humanas primarias y muestras de tejidos, los investigadores han encontrado que, probablemente, el virus se replica en los subgrupos de trofoblastos, en células endoteliales del feto y en macrófagos placentarios de Hofbauer. El acceso a estos tipos celulares puede verse potenciado mediante la unión de ZIKV a un receptor de superficie con actividad tirosina quinasa denominado AXL.
Tempranamente en el embarazo, la infección puede conducir a graves daños vasculares placentarios y a una reducción del flujo y de vasos sanguíneos. Alternativamente, el ZIKV puede cruzar la barrera placentaria sin causar un excesivo daño, propagándose hacia cerebro del feto, donde preferencialmente infecta y deteriora células progenitoras neuronales. Estos hallazgos pueden ser más típicos de una infección más tardía durante el embarazo, los que pueden deberse a una mayor producción de interferon-λ en los trofoblastos. La infección y la muerte de células neuroprogenitoras podrían inhibir la diferenciación de células neuronales, lo que explicaría el adelgazamiento cortical, la malformación de las estructuras cerebrales, y la microcefalia observada durante el embarazo en humanos.
Los investigadores deben tener en cuenta las diferencias morfológicas, espaciales, temporales durante el desarrollo placentario y cerebral entre roedores y los seres humanos. Sin embargo, muchos elementos de su desarrollo y las funciones celulares son similares en las dos especies. A pesar de que la escala de tiempo difiere sustancialmente, los procesos de desarrollo neuronal entre ambos son notablemente semejantes. En conjunto, los resultados de los estudios en ratones apoyan la hipótesis de que el contagio con ZIKV durante el embarazo causa la infección de la placenta y lesiones, y por otro lado apoyan la noción de que el ZIKV se propaga hacia cerebro fetal, eliminando células progenitoras neuronales, lo que probablemente contribuye a la microcefalia y a otras malformaciones congénitas observadas en neonatos humanos. Estos modelos de estudio en animales proporcionan una base para la definición de los mecanismos de patogénesis y representan un recurso para determinar los efectos de la variación de cepas del ZIKV sobre las manifestaciones clínicas y potencialmente permitirá además probar agentes terapéuticos y vacunas.
Fuente bibliográfica
Modeling Zika Virus Infection in Pregnancy
Indira U. Mysorekar, Ph.D., and Michael S. Diamond, M.D., Ph.D.
Department of Pathology and Immunology, Washington University School of Medicine, St. Louis.
DOI: 10.1056/NEJMcibr1605445
Temas Relacionados