Un actor clave subestimado en anafilaxia alimentaria
Los leucotrienos cisteinílicos juegan un papel crucial en esta condición, afectando la permeabilidad intestinal y la activación de mastocitos, lo que subraya la necesidad de nuevas estrategias terapéuticas para mejorar su manejo y prevención.
Las manifestaciones de la anafilaxia alimentaria van desde síntomas gastrointestinales y cutáneos leves hasta un compromiso sistémico potencialmente letal, caracterizado por reacciones de hipersensibilidad inmediata mediadas por inmunoglobulina E (IgE), donde los mastocitos y basófilos son las principales células efectoras. A pesar de los avances en la prevención y el tratamiento, la anafilaxia severa por exposición accidental a alérgenos alimentarios persiste.
El Dr. Joshua A. Boyce, del Brigham and Women's Hospital y la Universidad de Harvard en Boston, EE. UU., elaboró este artículo de revisión con el objetivo de resumir y analizar los hallazgos recientes sobre la participación crucial de los leucotrienos cisteinílicos (CysLTs) en la anafilaxia alimentaria. Esta investigación es esencial para esclarecer nuevos mecanismos patogénicos y resaltar sus importantes implicaciones clínicas y el desarrollo de futuras estrategias terapéuticas.
Se analizaron críticamente dos estudios clave en modelos murinos. El primero, de Hoyt y colaboradores, investigó la permeabilidad intestinal a alérgenos y la susceptibilidad a la anafilaxia experimental, evaluando la función de la dipeptidasa 1 (Dpep1), el leucotrieno D4 (LTD4) exógeno y los antagonistas de los receptores CysLTR1/2. El segundo estudio, de Bachtel y colaboradores, examinó la expansión de mastocitos mucosos intestinales y la respuesta anafiláctica en ratones BALB/c sensibilizados a ovoalbúmina, evaluando el impacto de los CysLTs endógenos y de fármacos como zileutón (inhibidor de la 5-lipoxigenasa) y montelukast (antagonista de CysLTR1).
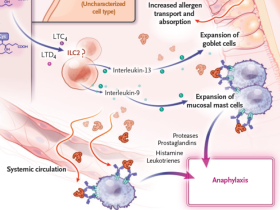
Los resultados destacan que los CysLTs, potentes mediadores lipídicos generados por mastocitos, células mieloides y epiteliales, son cruciales en la anafilaxia sistémica desencadenada por vía oral (figura 1). El equipo de Hoyt demostró que variantes del gen Dpep1, que metaboliza LTD4, afectan la susceptibilidad anafiláctica. Asimismo, el LTD4 exógeno aumentó la captación de proteínas alimentarias a través de vías de translocación de antígenos asociadas a células caliciformes (GAPs). La inhibición de la 5-lipoxigenasa o el antagonismo dual de CysLTR1/2 protegieron contra la anafilaxia inducida por vía oral, pero no por vía sistémica.
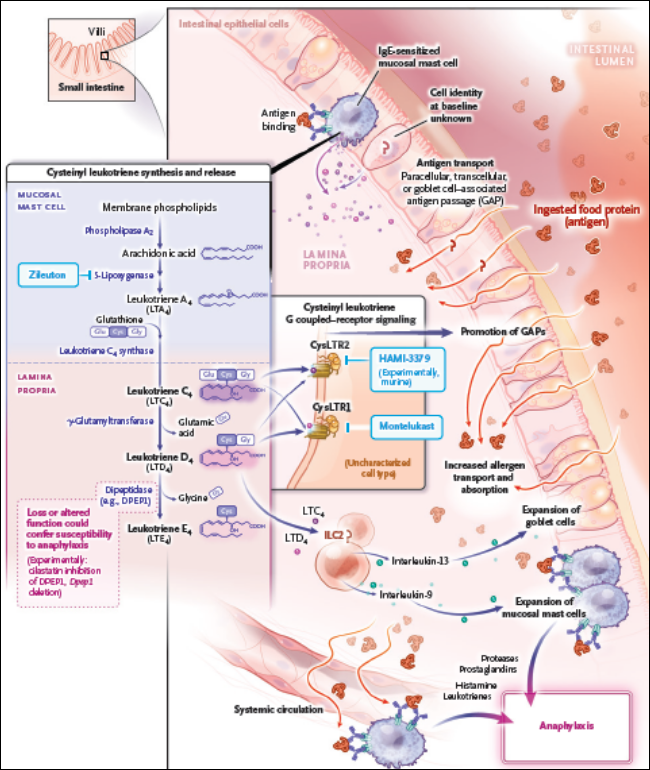
Figura 1. Mastocitos de la mucosa intestinal, leucotrienos cisteínicos y anafilaxia alimentaria.
La investigación de Bachtel y colaboradores reveló que la expansión y activación de mastocitos mucosos intestinales dependen de CysLTs endógenos de células hematopoyéticas. El tratamiento con zileutón previno tanto la expansión de mastocitos como los signos sistémicos de anafilaxia oral, y la deficiencia de CysLTR1 o CysLTR2 redujo la acumulación de mastocitos. Sin embargo, el montelukast no ofreció protección en este modelo, sugiriendo una complejidad en la interacción receptor-ligando. Los CysLTs también regulan la absorción sistémica de proteínas y el tiempo de tránsito gastrointestinal, impactando directamente la expansión de mastocitos y la función de la barrera intestinal.
En conclusión, los leucotrienos cisteinílicos, particularmente aquellos generados en el microambiente intestinal, desempeñan un papel fundamental y previamente subestimado en la patogenia de la anafilaxia inducida por alimentos. La susceptibilidad individual a esta condición es modulada por factores genéticos y ambientales que influyen en la vía de los CysLTs y la proliferación de mastocitos. A pesar de la existencia de terapias dirigidas a CysLTs, sus limitaciones actuales, como hepatotoxicidad o cobertura limitada de receptores, subrayan la necesidad imperativa de desarrollar nuevas estrategias farmacológicas.
Las implicaciones clínicas futuras incluyen el desarrollo o reposicionamiento de fármacos que logren una inhibición más eficaz y segura de la síntesis de CysLTs o un bloqueo más específico de sus receptores, con el objetivo de mejorar el manejo y la prevención de esta condición. Es crucial continuar la investigación con protocolos estandarizados de desafío oral o inmunoterapia para traducir estos hallazgos preclínicos a la práctica clínica.
Estos avances podrían conducir a la implementación de terapias complementarias a las estrategias actuales (ej. anti-IgE), enfocadas en modular la inmunidad de la mucosa y la integridad de la barrera intestinal, optimizando así el perfil de seguridad y eficacia del tratamiento.
Fuente bibliográfica
A New Stage for Seasoned Actors — Food Anaphylaxis and the Cysteinyl Leukotrienes
Joshua A. Boyce, M.D.
Brigham and Women’s Hospital & Harvard Medical School
N Engl J Med 2025; 393:2054-2057