Inmunoterapia dirigida al microambiente tumoral
Las características metabólicas de los tumores presentan considerables obstáculos para la función de células inmunitarias y la inmunoterapia. Sin embargo, mediante el uso de un antagonista de la glutamina, se logró desmantelar metabólicamente el microambiente inmunosupresor de los tumores. Se demostró que el bloqueo de glutamina en ratones portadores de tumores suprime el metabolismo oxidativo y glucolítico de las células cancerosas, lo que conduce a una disminución de la hipoxia, acidosis y agotamiento de nutrientes. En cambio, los linfocitos T efectores respondieron al antagonismo de la glutamina regulando notablemente el metabolismo oxidativo y adoptando un fenotipo de larga vida y altamente activado. Estos cambios divergentes en el metabolismo y la programación celular constituyen la base de potentes respuestas antitumorales. Por consiguiente, el antagonismo de la glutamina expone una diferencia previamente indefinida en la plasticidad metabólica entre las células tumorales y las células del sistema inmunitario que puede explotarse como "punto de control metabólico" para la inmunoterapia tumoral.
Antagonista JHU083
El crecimiento de los tumores se ve favorecido por las actividades metabólicas impulsadas por oncogenes que permiten a las células cancerosas absorber nutrientes, sintetizar macromoléculas y proliferar. Un objetivo de larga data de las investigaciones sobre el cáncer ha sido el de privar a los tumores de los nutrientes que suministran el metabolismo anabólico que promueve su crecimiento.
En ese sentido, Leone y colaboradores han informado recientemente que un nuevo antagonista de glutamina experimental, JHU083, induce la regresión del tumor en ratones evitando que las células cancerosas usen el aminoácido glutamina para alimentar su metabolismo anabólico (DOI: 10.1126/science.aav2588). Sorprendentemente, este fármaco no solo corta el suplemento nutricional al cáncer, sino que también condiciona el entorno del tumor para que se convierta en un microambiente más hospitalario para linfocitos T efectores, que, a su vez, amplían su ataque contra el tumor. Estos efectos culminan en la inmunidad antitumoral persistente, incluso cuando JHU083 se utiliza sin otros inmunomoduladores como un anticuerpo contra inhibidores de punto de control inmunitario (figura 1).
La privación de nutrientes es una terapia eficaz contra el cáncer en algunos contextos. Por ejemplo, las células de la leucemia linfoblástica aguda requieren una fuente exógena de asparagina, y el agotamiento de este aminoácido en la sangre -con el uso de la l-asparaginasa- ha sido un componente clave de la quimioterapia de la leucemia linfoblástica aguda durante décadas. La glucosa y la glutamina también están involucradas en el metabolismo de las células cancerígenas. Ambas son abundantes en el torrente sanguíneo, y su absorción por las células tumorales se incrementa a través de la señalización oncogénica. Una característica metabólica clásica de estas células anómalas es la rápida conversión de glucosa en lactato, seguido por la secreción de este último hacia el espacio extracelular, lo que proporciona tanto energía como sustratos para el metabolismo anabólico. La glutamina proporciona carbono y nitrógeno para las vías que sintetizan nucleótidos, glutatión y otras moléculas necesarias para el crecimiento de las células tumorales. Se han propuesto terapias para inhibir la glucosa y el metabolismo de la glutamina en los tumores, pero ninguna ha logrado ser aprobada.
¿Por qué ha sido tan difícil para los inhibidores metabólicos ganar tracción en la terapia del cáncer? Parte del problema es que pocas vías están realmente confinadas a las células malignas, y esto plantea la probabilidad de efectos tóxicos en células no malignas. Por eso los antifolatos que inhiben la síntesis de nucleótidos suprimen el crecimiento de los tumores, pero también inducen efectos tóxicos en la piel, la médula ósea, y otros tejidos con células proliferantes. La glucosa y la glutamina son nutrientes importantes que trafican carbono y nitrógeno entre los órganos, por lo que se predice que el bloqueo sistémico de su metabolismo afectará al cerebro, hígado, corazón y otros órganos.
Un segundo desafío es que el microambiente del tumor contiene una compleja mezcla de células malignas y no malignas. Nuestra comprensión de la cooperación y la competencia metabólica dentro de este microambiente es rudimentaria en el mejor de los casos, lo que dificulta la conceptualización de terapias que eliminen las células cancerosas sin dañar las células que limitan el crecimiento del tumor, en particular los linfocitos T y otros componentes celulares del sistema inmunitario. El extraordinario éxito de la inmunoterapia contra el cáncer implica que los inhibidores metabólicos necesitarán preservar La función de linfocitos T para tener eficacia clínica. Las sobrias observaciones iniciales indicaron que los linfocitos T también consumen grandes cantidades de glucosa y glutamina, al menos cuando son estimuladas a proliferar en cultivo.
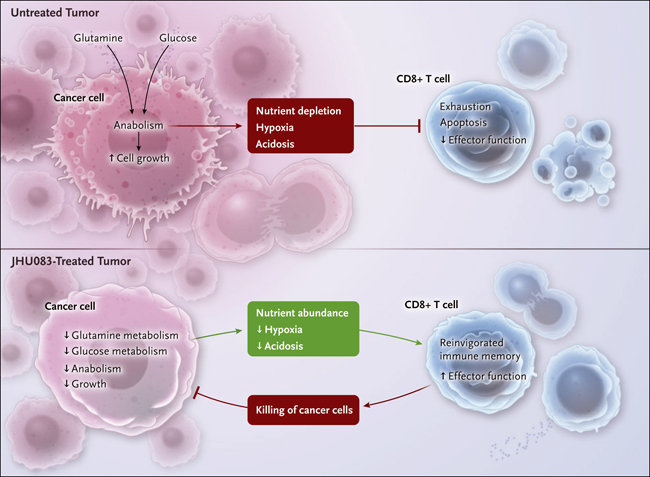
Figura 1. Agotamiento de los tumores mientras se potencia la función de las células T.
Leone y colaboradores informaron recientemente de que el JHU083, un antagonista del metabolismo de la glutamina suprime el crecimiento de las células tumorales y estimula la función antitumoral de los linfocitos T. Las células cancerosas toman glutamina, glucosa y otros nutrientes para apoyar su anabolismo (síntesis macromolecular) y el crecimiento. También acidifican el microambiente y agotan los nutrientes y el oxígeno, perjudicando la función de las células T CD8+ y evitando sus efectos citotóxicos. JHU083 provoca amplios efectos metabólicos en las células cancerosas, previniendo la absorción de glutamina y glucosa, limitando el crecimiento celular y dando paso a un microambiente favorable para la función efectora de las células T CD8+. Los linfocitos T en los tumores tratados con JHU083 (establecidos a partir de líneas de células cancerígenas de ratones) proliferan y muestran signos de memoria inmunológica y efectos citotóxicos mejorados contra las células cancerígenas, lo que en última instancia resulta en una potente inmunidad antitumoral.
¿Cómo enfrenta JHU083 estos desafíos? La carga útil de la droga es simple - 6-diazo-5-oxo-L-norleucina (DON), un análogo de la glutamina que inhibe las enzimas que utilizan este aminoácido como sustrato. Se sabe desde hace tiempo que DON mata las células cancerígenas, pero ha fallado en ensayos clínicos anteriores debido a los efectos tóxicos sistémicos. El JHU083 es un profármaco diseñado para liberar DON cuando es cortado por catepsinas y otras enzimas en tumores, limitando así su efecto en otros órganos.
Pero el mayor avance que representa el JHU083 es que inesperadamente ejerce efectos metabólicos diferenciales sobre las células cancerosas y linfocitos T en el microambiente del tumor. En las células cancerosas, la interrupción del metabolismo de la glutamina agota vías alimentadas por esta, como se esperaba. También perjudica la capacidad de las células cancerosas para absorber glucosa, cortando así dos combustibles principales de inmediato. Por el contrario, las células T son estimuladas por el fármaco, el que aumenta su infiltración en el tumor e induce programas de expresión génica indicativos de proliferación, mejora la supervivencia de las células, mejora la función del efector, y favorece la memoria antitumoral. Estos efectos se traducen en marcadas respuestas terapéuticas de un solo agente en modelos de ratones singénicos, en algunos casos completamente erradicando el tumor.
Fuente bibliográfica
Tumor Microenvironment, Metabolism, and Immunotherapy
Ralph J. DeBerardinis, M.D., Ph.D.
Howard Hughes Medical Institute and Children’s Medical Research Institute, University of Texas Southwestern Medical Center, Dallas.
DOI: 10.1056/NEJMcibr1914890