El factor infeccioso de la enfermedad celiaca
Se ha propuesto que las infecciones virales causan procesos patológicos que conducen a la respuestas inmunitarias tipo T helper 1 (TH1) contra el gluten de la dieta. Particularmente, el reovirus, es un patógeno avirulento que provoca inmunidad protectora, pero que también puede alterar la homeostasis intestinal al suprimir la conversión de células T periféricas reguladoras (pTreg) y promover un desarrollo de respuesta TH1 contra el antígeno dietético. Recientes hallazgos en modelos animales y estudios clínicos apoyan el rol de la infección reoviral aparentemente inocua, con el desarrollo de la enfermedad celíaca.
Reovirus inductores
La enfermedad celíaca, es un ejemplo de una enfermedad de la que se sabe mucho acerca de los aspectos genéticos y los factores ambientales que la producen. Sin embargo, un equipo de investigadores, liderado por Bouziat (Science. 2017 Apr 7;356(6333):44-50) han definido recientemente la "receta" que desencadena la enfermedad. Este equipo utilizó un virus humano recombinante y ratones transgénicos que expresan genes humanos que predisponen a la patología. Sus observaciones implican a reovirus en la patogénesis de la enfermedad celíaca. Su análisis de muestras de suero de pacientes mostró resultados consistentes con los del modelo animal, lo que sugiere que sus conclusiones son relevantes para la biología humana.
Como es cierto en todos los casos complejos de enfermedades mediadas por el sistema inmunitario, docenas de genes han sido implicados como contribuyentes potenciales a la enfermedad celíaca. También es válido para la mayoría de las enfermedades inmunomediadas, variantes en los genes HLA son los más importantes. A menos que el individuo exprese uno de los alelos críticos de HLA, es extremadamente improbable que alguna vez el cuerpo desarrolle sensibilidad al gluten. La principal función conocida de las moléculas HLA es permitir la presentación de antígenos de una célula, como una célula dendrítica o un macrófago a otras como un linfocito T, para que éste pueda hacer frente a un antígeno mediante una respuesta inmune específica. HLA-DQ2 y HLA-DQ8 designan proteínas que tienen una asociación conocida con la enfermedad celíaca. Estas proteínas activan las células T presentando un fragmento de péptido derivado del gluten. Este fragmento es creado por la actividad enzimática de la transglutaminasa 2, que es también el auto antígeno selectivo utilizado en el cribado de posible enteropatía sensible al gluten.
Posiblemente para la enfermedad celíaca, la receta está completa: un gen en forma de HLA, un factor ambiental (la ingesta de gluten derivado de varios granos), y una enzima endógena que cataliza la formación de antígenos y sirve como un autoantigeno transeúnte en el proceso. Y la combinación debería resultar en el cambio característico de atrofia vellosa en el intestino delgado. Pero esta lista de ingredientes debe estar incompleta, ya que la enfermedad celíaca no se desarrolla en el 95 al 98% de las personas que portan alelos codificantes para HLA-DQ2 o HLA-DQ8. Bouziat y sus colegas encontraron que un ingrediente perdido podría ser un reovirus.
Los reovirus no son virulentos en el ratón. Infectan el intestino sin causar ningún síntoma. El equipo de investigación infectó por separado ratones con dos reovirus similares, una cepa llamada Lang y con un resortante generado a partir de una cepa llamada Dearing. El virus Lang activa células dendríticas en el intestino delgado, mientras que la el virus Dearing no lo hace. Los dos virus también difieren en su capacidad de inducir la transcripción del factor regulador de interferón 1 (IRF1), que es potencialmente la diferencia crítica.
Cuando los ratones transgénicos que expresan HLA-DQ8 fueron infectados con Lang y luego alimentados con gluten, se generaron anticuerpos contra el gluten y una activación de la transglutaminasa en el intestino delgado. En contraste, los ratones transgénicos infectados con Dearing no tuvieron estas respuestas. Los autores también encontraron que pacientes con enfermedad celíaca eran más propensos a tener anticuerpos que los controles sanos, aunque el significado de este hallazgo fue al límite. Sin embargo, un subgrupo de pacientes con la enfermedad celíaca tenía niveles mucho más altos de anticuerpos contra el reovirus que los controles. Estos individuos también tenían una expresión desrregulada de IRF1, fenómeno que apoya un rol de la infección por reovirus en este subgrupo de personas. Una variedad de otras infecciones virales como la causada por rotavirus probablemente pueden servir como cofactores para activar la respuesta inmune intestinal y crear una predisposición a la enfermedad celíaca.
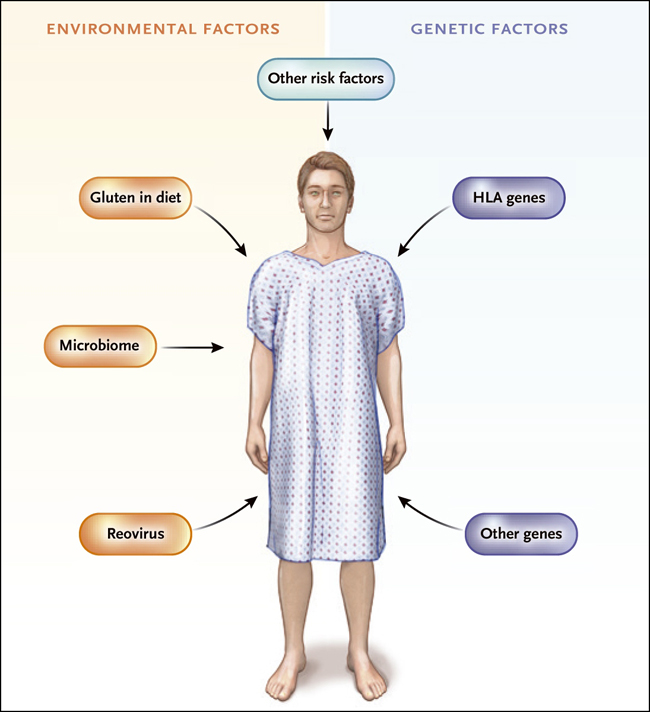
Figura 1. Susceptibilidad a la enfermedad celíaca.
La mayoría de las enfermedades autoinmunes e inmunitarias son el resultado de una combinación de factores genéticos y ambientales. En el caso de la enfermedad celíaca, contribuyentes como HLA-DQ2 y HLA-DQ8 y la ingesta de gluten en la dieta son esenciales. Sin embargo, estos factores no son suficientes, ya que existen otros componentes genéticos (por ejemplo, algunos que afectan a las citocinas y otros que afectan a la inmunidad innata) y los ambientales (por ejemplo el microbioma). Bouziat y sus colegas descubrieron recientemente que una infección por reovirus podría ser un factor ambiental crítico. La etiqueta "otros factores de riesgo "se ha incluido en la figura porque, al menos en el ratón una combinación de la composición genética HLA-DQ8, gluten en la dieta, e infección por reovirus fue insuficiente para causar el característico cambio de la estructura vellosa en el intestino delgado.
La fórmula descrita es una simplificación. HLA es el gen más importante en relación con la enfermedad celíaca, pero no es el único. Factores adicionales que se han implicado en el desarrollo de la enfermedad celíaca incluyen el microbioma bacteriano, el sistema inmune innato, citoquinas (por ejemplo, interleucina-15), y la enzima fucosiltransferasa 2. Además, la combinación de la infección con cepa reoviral Lang, el transgen HLA, y la alimentación con gluten, produjo anticuerpos contra éste pero no atrofia vellosa, lo que indica que en el modelo descrito por Bouziat sigue faltando un "ingrediente" en la receta para un verdadero modelo de la enfermedad celíaca (figura 1).
Sin embargo, está claro que en el ratón, por lo menos, un virus que por sí solo no causa síntomas puede combinarse con factores genéticos y otros componentes ambientales que pueden resultar en una posible respuesta inmune dañina. Y no es difícil extrapolar los hallazgos sobre la enfermedad celíaca a otras enfermedades que son influenciadas por un fuerte efecto de HLA clase II, como la diabetes tipo 1, artritis reumatoide y lupus sistémico. Si un el virus es una parte esencial como desencadenante, prevenir o tratar la infección viral puede convertirse en una profilaxis eficaz. Por lo que posiblemente la vacunación podría bloquear el desarrollo de la autoinmunidad.
Fuente bibliográfica
Celiac Disease and Autoimmunity — The Missing Ingredient
James T. Rosenbaum, M.D.
Legacy Devers Eye Institute and Oregon Health and Science University, Portland.
DOI: 10.1056/NEJMcibr1706917
Temas Relacionados