Células T reguladoras en la esclerosis múltiple
Estas células suprimen la inflamación y son defectuosas en las enfermedades autoinmunes. Un estudio reciente aporta nuevos conocimientos sobre cómo se desregulan en la esclerosis múltiple y apunta a una posible estrategia para restaurar su función.
La autoinmunidad se produce cuando el sistema inmunitario se vuelve crónicamente desregulado. En prácticamente todas las enfermedades autoinmunes, susceptibilidad genética y factores ambientales convergen para iniciar la patogénesis. La comprensión de la interacción entre los genes y el medio ambiente es la base para identificar nuevas estrategias terapéuticas, que son cada vez más necesarias debido a la creciente incidencia de la autoinmunidad en las sociedades industrializadas. Se ha prestado mucha atención en las células T reguladoras, que son defectuosas en muchas enfermedades autoinmunes, incluida la esclerosis múltiple. Un informe reciente de Pompura y colaboradores, proporciona una nueva visión de cómo las células T reguladoras se desregulan en la esclerosis múltiple y señala una potencial estrategia para restaurar su función.
Las células T ingenuas encuentran antígenos derivados de patógenos en los tejidos linfoides y se diferencian en células T efectoras. Existen múltiples tipos de células T efectoras que, mediante distintos mecanismos erradican diferentes clases de organismos infecciosos. La programación transcripcional regida por factores de transcripción maestros determina en gran medida el fenotipo funcional de la célula T. Las células T efectoras suelen detectar patógenos y ejecutar su función efectora en los tejidos; las células T reguladoras desempeñan un papel fundamental en la resolución de la respuesta inflamatoria. Algunas células T efectoras permanecen en el tejido y se convierten en células T de memoria residentes para proporcionar una rápida protección contra la reinfección del patógeno. Las células T reguladoras también permanecen en los tejidos, donde su función no es solo regular la posible reactivación de las células T efectoras, sino también promover la cicatrización de heridas y mantener la homeostasis de los tejidos.
Distintos subconjuntos de células T se asocian con diferentes estados metabólicos, lo que sugiere que los procesos metabólicos y la programación transcripcional dentro de la célula se coordinan para determinar el fenotipo funcional. Las células T ingenuas quiescentes generan ATP a través de la fosforilación oxidativa (OXPHOS) impulsada por la β-oxidación de los ácidos grasos (FAO). Al activarse, las células T cambian a glucólisis aeróbica, un proceso que se adapta mejor a las demandas energéticas de la división celular. La programación metabólica es compleja en las células T reguladoras, porque las células de este subconjunto pueden cambiar de estado metabólico en diferentes etapas de su vida y en diferentes microambientes. Aunque la glucólisis parece ser requerida para el desarrollo de las células T reguladoras en los seres humanos, la expresión de FoxP3, el factor de transcripción maestro que dirige la función de las células T reguladoras, suprime los genes relacionados con la glucólisis e induce los genes relacionados con la OXPHOS impulsada por la FAO que son necesarios para la máxima supresión de las células T efectoras. La capacidad de las células T reguladoras de cambiar entre diferentes programas metabólicos puede mejorar su capacidad de preservar la función supresora mientras se adaptan a los diferentes sustratos metabólicos que se encuentran en los microambientes de los tejidos. Sin embargo, las señales específicas de los tejidos que permiten a las células T reguladoras residentes en ellos preservar la función supresora no están bien definidas y pueden ser fundamentales para entender cómo pueden desregularse.
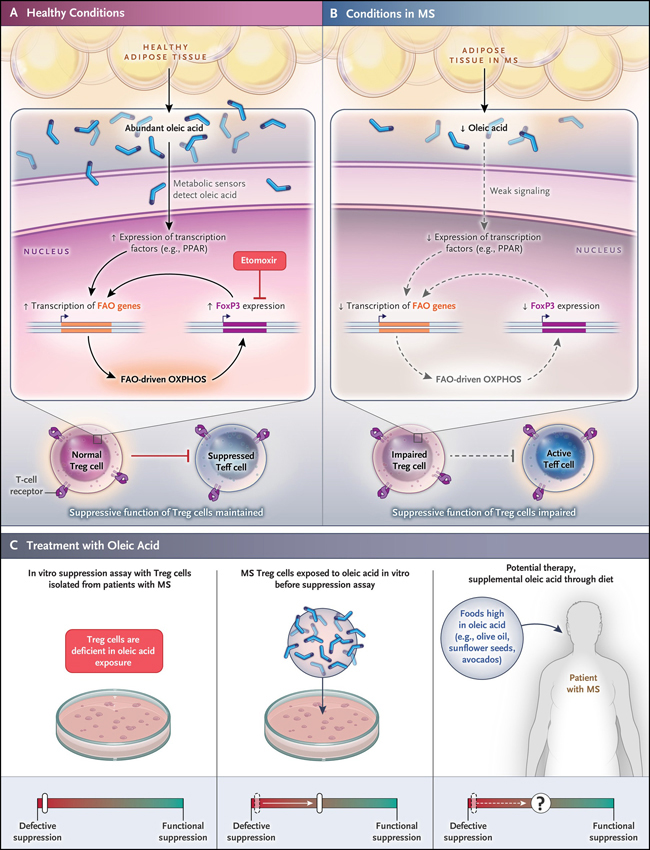
Figura 1. Ácido oleico como mediador de OXPHOS impulsada por FAO, expresión de FoxP3 y la actividad de las células T reguladoras.
Las células T reguladoras (Treg) del tejido adiposo sano perciben el ácido oleico y aumentan la expresión de factores de transcripción que promueven la expresión de genes necesarios para la la fosforilación oxidativa (OXPHOS) impulsada por la β-oxidación de los ácidos grasos (FAO). Esta vía metabólica aumenta y estabiliza la expresión de FoxP3, potenciando la función supresora de las células Treg. La OXPHOS impulsada por la FAO es necesaria porque, el etomoxir, un inhibidor de la OXPHOS impulsada por la FAO, bloquea el aumento de FoxP3 impulsado por ácido oleico. FoxP3 también aumenta la expresión de los genes que apoyan la OXPHOS impulsada por FAO, estableciendo un potencial loop de retroalimentación positiva (Panel A). Una menor concentración de ácido oleico en el tejido adiposo de pacientes con esclerosis múltiple (EM) compromete la señalización metabólica inducida por este ácido graso de cadena larga y se correlaciona con el deterioro de la función de las células T reguladoras (Panel B). En pacientes con esclerosis múltiple, el tratamiento con ácido oleico in vitro restaura parcialmente la función supresora de las células T reguladoras, un hallazgo que plantea la posibilidad de que este efecto pueda lograrse in vivo mediante una dieta enriquecida con ácido oleico (Panel C).
La observación de que la actividad supresora de las células T reguladoras es mayor durante la OXPHOS impulsada por la FAO llevó a Pompura y colaboradores a plantear la hipótesis de que las células T reguladoras conservan su función supresora en los tejidos al permitir que la detección metabólica del ácido graso de cadena larga más abundante en el tejido impulse la transcripción de FoxP3. Encontraron que el ácido oleico era el más abundante en el tejido adiposo humano. Los investigadores expusieron in vitro células T reguladoras aisladas del tejido adiposo a varios ácidos grasos de cadena larga y encontraron que sólo el ácido oleico aumentaba la expresión de FoxP3. Encontraron que la OXPHOS impulsada por la FAO era necesaria para el aumento de la expresión de FoxP3, demostrando que la adición de etomoxir, un inhibidor de la FAO-OXPHOS, eliminaba el efecto del ácido oleico. Este acido desencadenó un aumento de los factores de transcripción que promueven expresión de los genes de la vía FAO, lo que en última instancia resulta en un aumento de la expresión de FoxP3 y una mayor actividad supresora. Interesantemente, se ha reportado de que el propio FoxP3 promueve la expresión de genes relacionados con la OXPHOS, creando potencialmente un loop de retroalimentación positiva entre la captación de lípidos y la expresión de FoxP3 en el tejido adiposo.
Para evaluar la relevancia de sus observaciones in vitro, Pompura y colaboradores analizaron el transcriptoma (la gama completa de moléculas de ARN expresadas en una célula determinada) de células T reguladoras expuestas in vitro a ácido oleico o ácido araquidónico (un ácido graso con actividad proinflamatoria). Compararon estas firmas transcriptómicas con las de las células T reguladoras obtenidas de sangre y tejido adiposo de donantes sanos y de pacientes con esclerosis múltiple. Los investigadores descubrieron que el transcriptoma de las células T reguladoras generado por la exposición al ácido oleico se asemejaba más al perfil de expresión de las células T reguladoras derivadas de la sangre y del tejido adiposo de los donantes sanos que al de los pacientes con esclerosis múltiple, mientras que el perfil de expresión de las células T reguladoras derivadas del tejido adiposo de los pacientes con esclerosis múltiple se parecía más al perfil transcriptómico inducido por el ácido araquidónico.
Intrigantemente, Pompura y colaboradores encontraron que la concentración de ácido oleico en el tejido adiposo era menor en los pacientes con esclerosis múltiple que en las personas sanas y que la exposición de las células T reguladoras de los pacientes con esclerosis múltiple al ácido oleico remedia parcialmente los defectos en la función supresora (Figura 1). Aunque este estudio presenta algunas salvedades, ya que los pacientes con esclerosis múltiple eran mayores y tenían un índice de masa corporal medio más elevado que las personas sanas, estas observaciones sugieren que la composición lipídica del tejido adiposo puede influir en la potencia de las células T reguladoras para suprimir la inflamación.
Estos resultados plantean más preguntas. ¿Están los niveles más bajos de ácido oleico en el tejido adiposo asociados a otras enfermedades autoinmunes? ¿Puede aumentarse la concentración de ácido oleico en el tejido adiposo mediante la administración de suplementos dietéticos y, de ser así, aumentaría la actividad supresora de las células T reguladoras en circulación? ¿Interactúa la deficiencia de ácido oleico con la susceptibilidad genética a las enfermedades autoinmunes? En caso afirmativo, ¿podría el descubrimiento de tales interacciones implicar nuevas dianas terapéuticas? ¿La composición lipídica de los tejidos como el líquido cefalorraquídeo y el tejido cerebral en pacientes con esclerosis múltiple también influye la potencia de las células T reguladoras? Son necesarias investigación futura para responder a estas preguntas.
Fuente bibliográfica
Regulatory T Cells in Multiple Sclerosis
Joan M. Goverman, Ph.D.
Department of Immunology, University of Washington, Seattle.
N Engl J Med 2021; 384:578-580