Bloqueo del tránsito depresivo
Los transportadores de serotonina son proteínas integrales de membrana capaces de recaptar este neurotransmisor desde el espacio sináptico hacia el interior de las células. Este fenómeno celular, se relaciona con casos de cuadros depresivos y variados trastornos neurológicos. Los avances en esta materia son el reflejo de análisis estructurales de estas proteínas transportadoras, lo que ha permitido identificar un sitio de unión a fármacos que compiten con la serotonina, evitando el reingreso del neurotransmisor y aumentando su disponibilidad durante la sinapsis. Interesantemente, estas moléculas, conocidas como inhibidores selectivos de recaptación de serotonina, además pueden acoplarse a un segundo sitio - denominado alostérico- presente en el transportador. Esta unión, permite aumentar la afinidad del fármaco asociado al sitio principal y como consecuencia, potenciar el efecto inhibitorio. Estos enfoques basados en la biología estructural de proteínas tan relevantes, ofrecen nuevas oportunidades terapéuticas para las complicaciones del sistema nervioso central.
Transportador de serotonina
En un reciente artículo, Jonathan A. Coleman y colaboradores (Nature. 2016 Apr 21;532(7599):334-9) describieron la primera estructura de alta resolución del transportador de serotonina (SERT). Esta proteína, recaptura moléculas de serotonina que han sido liberadas por la célula y, de esta forma, modula los efectos de este importate neurotransmisor en neuronas vecinas. Quienes no estén familiarizados con SERT podrían preguntarse si determinar su estructura molecular es algo relevante. En primer lugar, es técnicamente un desafío purificar grandes cantidades de SERT requeridas para el análisis estructural. En segundo lugar, la visualización de la estructura molecular detallada de una proteína de este tipo, podría proporcionar oportunidades sin precedentes para desarrollar terapias más selectivas y eficaces para enfermedades como la depresión.
Los neurotransmisores serotonina, dopamina y noradrenalina son liberados desde neuronas particulares y cruzan la hendidura sináptica para unirse a los receptores de neuronas vecinas, en las que modulan los efectos de señales inhibitorias o excitatorias de otros neurotransmisores. El SERT, junto con los transportadores de dopamina (DAT) y de noradrenalina (NET), pertenece a la familia de proteínas de transporte de neurotransmisores sodio symporter (NSS), que a su vez es parte de la segunda mayor clase de proteínas integrales de membrana en mamíferos. Es decir, proteínas que movilizan iones, pequeñas moléculas y nutrientes dentro y fuera de las células. Los SERT, DAT y NET son expresados selectivamente en la superficie de neuronas presinápticas y, mediante la recaptación de serotonina, dopamina y noradrenalina de vuelta a la célula, actúan terminando los efectos moduladores de tales neurotransmisores.
Estudios de silenciamiento génico realizados hace casi 20 años, muestran que los tres transportadores desempeñan un rol esencial en el mantenimiento diario del control de la señalización neuronal. Su relevancia se ha destacado, además, por el descubrimiento de mutaciones raras en genes codificantes para tales proteínas transportadoras, anomalías que se han vinculado a enfermedades como el autismo, el trastorno de hiperactividad con déficit de atención (THDA) y Parkinson.
Drogas como la cocaína, las anfetaminas y el éxtasis, ejercen su acción psicoestimulante por medio del secuestro de las proteínas transportadoras. Por otro lado, medicamentos que se dirigen a SERT, NET y DAT, son utilizados para tratar la depresión y el TDAH, entre otras condiciones. Los antidepresivos, incluyendo los inhibidores selectivos de la recaptación de serotonina (ISRS) y los de noradrenalina y serotonina (IRSN), bloquean los transportadores, evitando la recaptación del neurotransmisor y, por lo tanto, aumentan su disponibilidad y actividad global en la sinapsis. En teoría, así es cómo los ISRS y los IRSN alivian algunos de los síntomas de la depresión y otras condiciones relacionadas con el estado de ánimo.
En 2005, el grupo que lleva a cabo los estudios actuales, determinó la estructura de LEUT, un pariente bacteriano de SERT. El transportador de leucina (LEUT) participa en la absorción de nutrientes en estos organismos unicelulares y funciona de manera similar a SERT. En 2013, los investigadores también identificaron la estructura de DAT en la mosca de la fruta. Este estudio sugiere que la organización estructural de estas proteínas es altamente conservada evolutivamente, y por otro lado, define elementos estructurales que indican que el mecanismo por el que los NSS transportan sustratos también es conservado. Al proporcionar conocimientos moleculares sobre la estructura del SERT en humanos, el presente estudio confirma que la naturaleza, cuando encuentra una manera de hacer algo, lo hace una y otra vez. Pero en el caso de SERT, existe un interesante giro a este fenómeno.
Para identificar estructuras en alta resolución usando cristalografía de rayos X, las proteínas deben ser purificadas en grandes cantidades. Las proteínas transmembrana son notoriamente difíciles de purificar, porque son inestables una vez retiradas del ambiente hidrófobo de la bicapa lipídica. Previamente, las proteínas de membrana se estabilizaban con éxito mediante la introducción de mutaciones, induciendo la formación de un complejo con proteínas fácilmente cristalizables, o incluso mediante el desarrollo de anticuerpos para la estabilización de las proteínas nativas. Coleman y sus colegas, utilizaron un escaneo cuidadosamente elaborado para identificar unos pocos residuos de aminoácidos que podrían ser mutados para estabilizar al SERT, para purificarlo sin afectar sus propiedades funcionales. Los cristales resultantes, revelaron que más de 600 residuos aminoacídicos de SERT se enhebran unas 12 veces a través de la membrana para formar una estructura 3D diseñada para mediar el transporte de neurotransmisores acoplados a iones.
Los autores utilizaron cristalografía de rayos X para determinar las estructuras del SERT unidos a dos ISRS: paroxetina y escitalopram (el S-enantiómero de citalopram). Encontraron una molécula de paroxetina unida fuertemente en el centro de la cavidad del SERT, localizada profundamente dentro de la membrana plasmática. Como consecuencia, se bloquea competitivamente el transporte de serotonina. Sin embargo, dos moléculas de escitalopram se unen al SERT: una, como la paroxetina, lo realiza con una alta afinidad de la cavidad central, y la segunda más libremente en un vestíbulo orientado hacia el exterior (fig. 1).
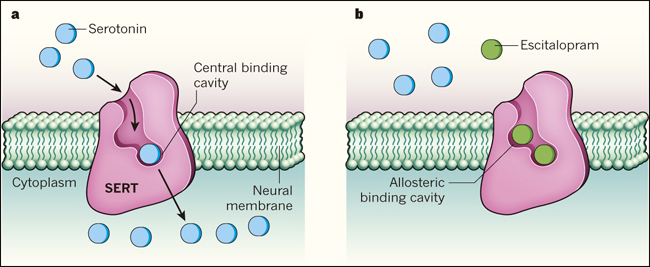
Figura 1. Bloqueo antidepresivo de una proteína transportadora.
a, La molécula neurotransmisora, serotonina, es captada por las neuronas mediante la proteína transportadora de serotonina (SERT), a través de una unión de alta afinidad en una cavidad central. b, Coleman y colegas identificaron las estructuras del SERT unidas a dos antidepresivos: paroxetina o escitalopram (sólo se muestra escitalopram). Ambos fármacos se unen a la cavidad central, bloqueando el transporte de serotonina, al competir con el neurotransmisor por el sitio de unión. Escitalopram también se une en un segundo sitio, denominado alostérico, que se cree que prolonga la unión en el sitio central, mejorando la eficacia del bloqueo farmacológico del SERT.
La existencia de un segundo sitio de unión (conocido como alostérico) aparte del principal, se propuso hace más de 30 años. En 2012, el modelado y experimentos de mutación, sugirieron que el sitio se encuentra orientado hacia el exterior, tal como Coleman y colegas confirman. Los estudios previos sugirieron que, cuando está presente en concentraciones suficientemente altas, la unión de escitalopram en el sitio alostérico, podría retardar notablemente la disociación de fármacos unidos al sitio de alta afinidad - prolongando así la actividad inhibitoria del medicamento. Este fenómeno "modificador alostérico positivo" se ha propuesto para explicar la superior eficacia clínica del escitalopram en comparación con otros ISRS, pero confirmar tal mecanismo en estudios con animales ha sido difícil. A pesar de esto, la documentación molecular acerca del sitio alostérico es de gran relevancia dado que su estructura podría proporcionar oportunidades no apreciadas previamente para el desarrollo de fármacos selectivos.
La presencia de sitios alostéricos en proteínas de membrana podría ser más común de lo previsto. Un ejemplo de la potencialidad de este hallazgo proviene de los receptores acoplados a proteína G (GPCR, por sus siglas en inglés) - proteínas de membrana que unen serotonina, dopamina, noradrenalina, y muchas otras moléculas de señalización en neuronas postsinápticas. La determinación exitosa de las estructuras de más de dos docenas de estos receptores ha posibilitado el hallazgo de muchos sitios de unión alostéricos potenciales que están siendo aprovechados para desarrollar modificadores positivos o negativos de señalización para combatir enfermedades. La misma oportunidad ahora podría presentarse para los transportadores. La visualización de la dinámica funcional de estas proteínas, junto con el modelado molecular de unión de diferentes fármacos, ofrece oportunidades sin precedentes para el desarrollo de mejores tratamientos para los trastornos del sistema nervioso central.
Fuente bibliográfica
Structural Biology: Antidepressants at work
Marc G. Caron & Ulrik Gether
Departments of Cell Biology, Medicine and Neurobiology, Duke University Medical Center, Durham, North Carolina 27710, USA.
doi:10.1038/nature17883
Temas Relacionados