ARN y una nueva terapéutica
Una reciente revolución en la biología del ARN ha llevado a la identificación de nuevas clases con funciones imprevistas y nuevos tipos de modificaciones del ARN. También se ha descubierto una inesperada multiplicidad de transcripciones alternativas y una amplia actividad transcripcional de regiones extragénicas. Este desarrollo en la biología básica del ARN ha generado una revolución en las estrategias basadas este ácido nucleico con fines terapéuticos. Debido a que nuevos medicamentos basados en ARN se dirigen a la regulación de procesos traduccionales en lugar de proteínas u otros receptores farmacológicos, esta nueva clase terapéutica promete ampliar en gran medida el dominio de los blancos terapéuticos más allá de lo que se puede lograr con moléculas pequeñas y productos biológicos.
ARN no codificantes
El Premio Lasker-Koshland 2018 al Logro Especial en Ciencias Médicas, anunciado el 11 de septiembre, reconoce a Joan A. Steitz, quien ha hecho contribuciones pioneras a la comprensión de la biología del ARN y, que como científica, ha liderado el camino mostrando un modelo a seguir como una firme defensora para promover el avance de mujeres y minorías en la comunidad científica.
Steitz comenzó su formación científica cuando había pocas mujeres en la ciencia, no mucho después del descubrimiento del "dogma central" de la biología molecular. El dogma central postula que el ADN proporciona la información codificante para los genes, que se transcriben en ARN mensajero (ARNm) que luego se traducen por ribosomas en proteínas. Como investigadora postdoctoral y miembro joven de la facultad, identificó las secuencias de ARNm que los ribosomas reconocen para comenzar la traducción y encontró que el reconocimiento del sitio de inicio se basa en el apareamiento de bases entre las regiones de ADN restringidas por secuencias localizadas cerca del codón de inicio y una secuencia complementaria en un ARN ribosomal.
Según el dogma central, el ARN tiene un papel pasivo e intermediario como mensajero, llevando información codificada en el ADN a proteínas, que son los principales componentes estructurales y enzimáticos de las células. Sin embargo, desde que este dogma se conceptualizó por primera vez, el mundo del ARN ha explotado -en parte como consecuencia de los avances en la tecnología de secuenciación profunda- para abarcar un universo diverso de ARNs que se modifican de cientos de formas y se transportan a diferentes lugares de la célula con innumerables funciones más allá de la codificación de proteínas (figura 1).
De hecho, los ARNm constituyen sólo un pequeño porcentaje del ARN celular. En los eucariontes, las secuencias de la mayoría de los transcritos primarios de ARNm, llamados pre ARNm, contienen regiones codificantes (exones) y secuencias intermedias (intrones) que necesitan ser removidas antes de la traducción en un proceso llamado empalme, el cual ocurre a medida que el ADN está siendo transcrito en preARNm. La mayor parte de los ARNs celulares son no codificantes (es decir, ARNs que no se traducen en proteínas), que van desde aproximadamente veinte a miles de nucleótidos de longitud. Estos ARNs no codificantes son componentes centrales de las ribonucleoproteínas que funcionan como máquinas celulares para regular la transcripción, orquestar el procesamiento y la traducción del ARN postranscripcional (y otras funciones), y utilizar el apareamiento de bases de ácido nucleico con otros ARNs o ADNs para conferir una exquisita especificidad de secuencia a sus blancos. Steitz jugó un papel clave en descubrir muchas funciones ARNs pequeños no codificantes. También fue clave en dilucidar los pasos necesarios para procesar los transcritos primarios de estos ARN y convertirlos en parte funcional de la maquinaria del ARN celular.
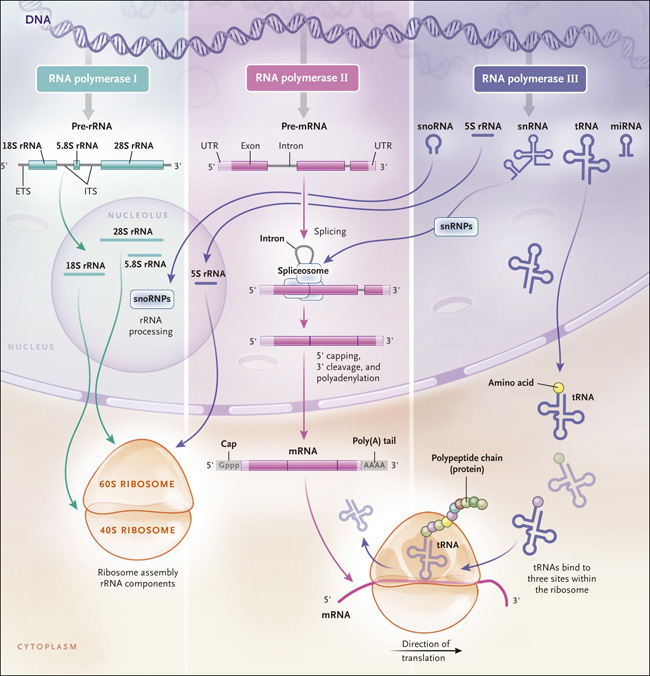
Figura 1. La abundancia de ARN.
El ADN es transcrito por tres enzimas diferentes - ARN polimerasas - en transcritos primarios o precursores (preARNs) de ARN mensajero (los preARNs son producidos por la ARN polimerasa II) y ARN pequeños y grandes no codificantes. Los ARN pequeños no codificantes, se incorporan a la maquinaria de ribonucleoproteínas (RNP). Los ARN ribosomales (ARNr), los componentes de ARN del ribosoma, son críticos para traducir los ARNm en proteínas. El transcrito principal de ARNr, que codifica tres de los cuatro ARNr (5.8S, 18S y 28S), es sintetizado por la RNA polimerasa I y procesado en el nucleolo con el uso de pequeñas RNP nucleolares (snoRNPs). El cuarto ARNr (5S) es sintetizado por la RNA polimerasa III. Los ARN pequeños no codificantes (snRNAs, por sus siglas en inglés) sintetizados por la RNA polimerasa III incluyen snRNAs que empalman los preARNm dentro de un complejo grande y dinámico llamado espliceosoma; pequeños ARNs nucleolares que procesan ARNr y otros ARN no codificadores; ARN de transferencia (tRNAs) que cargan aminoácidos en péptidos incipientes en el ribosoma; y pre-microRNAs. Los pre-microARNs son procesados en microARNs (miRNAs) en el núcleo; los miRNAs regulan la expresión génica causando la degradación del ARNm o bloqueando el inicio de su traducción en el citosol. ETS denota espaciador transcribible externo, Gppp trifosfato de guanosina , ITS espaciador transcribible interno y UTR región no traducida.
También descubrió el papel de los ARN pequeños no codificantes en la promoción de los ciclos replicativos virales, y realizó importantes contribuciones a la comprensión de cómo los ARN pequeños no codificadores llamados microARN, que suprimen la expresión de los genes huéspedes y virales mediante la promoción de la descomposición del ARNm y el bloqueo de la traducción de las proteínas, son procesados y regulan la expresión de los genes. Aunque la mayoría de los biólogos se habían concentrado previamente en la regulación de la transcripción (mediante proteínas llamadas factores de transcripción) como el "control" primario de la expresión de las proteínas, cada vez está más claro que los procesos mediados por el ARN tienen, en conjunto, un papel igualmente importante. Estos procesos incluyen la regulación transcripcional y la regulación postranscripcional del empalme; modificaciones del ARNm, como la metilación y la poliadenilación; la unión de regiones de ARNm no traducidas a proteínas que secuestran los ARNm en sitios subcelulares especializados; y la descomposición del ARNm. De hecho, los dos sistemas - factores de transcripción y ARNs no codificadores - se regulan mutuamente.
La clave que desbloqueó el mundo de los ARN pequeños no codificantes fue el descubrimiento por Steitz y uno de sus estudiantes (Michael Lerner) de que algunos anticuerpos antinucleares, generados en pacientes con lupus eritematoso sistémico y otras enfermedades autoinmunes, reconocen selectivamente tanto los componentes proteicos como los del ARN de muchas de las abundantes ribonucleoproteínas. El laboratorio Steitz usó los autoanticuerpos para aislar o agotar tipos específicos de ribonucleoproteínas con el fin de identificar sus componentes y diseccionar su función.
Los conocimientos de los estudios pioneros de Steitz que revelaron el mundo de los ARN pequeños y cómo funciona están empezando a traducirse en nuevas clases de terapéutica. El año 2017, dos fármacos basados en oligonucleótidos antisentido de ARN, nusinersen y eteplirsen, que alteran el splicing del ARN, fueron aprobados para tratar enfermedades neurodegenerativas que antes no eran tratables (atrofia muscular espinal y distrofia muscular de Duchenne, respectivamente). El primer medicamento que aprovecha la vía de microARN de interferencia de ARN, patisiran, acaba de ser aprobado para desintegrar el ARN para el tratamiento de una forma hereditaria de amiloidosis. Estos son probablemente los primeros ejemplos de una nueva farmacopea de medicamentos basados en el ARN que ampliará el universo de dianas de los medicamentos más allá del uso de pequeñas moléculas y agentes biológicos.
El premio Lasker-Koshland también reconoce el trabajo inspirador de Steitz como modelo, mentor y defensor de las mujeres en la ciencia. Cuando Steitz ingresó a la escuela de postgrado, había muy pocas mujeres en ciencia. Las mujeres que triunfaron como científicas tenían que ser excepcionalmente capaces y decididas. Como dijo Steitz en un artículo del New York Times en 2001, "Si una mujer es una estrella no hay tantos problemas. Si es tan buena como el resto de los hombres, es realmente horrible. Se espera que una mujer sea el doble de buena por menos". La situación de las mujeres en la ciencia ha mejorado mucho desde entonces, por lo que la discriminación flagrante es poco común. Sin embargo, el campo de juego está lejos de ser parejo, debido al sesgo inconsciente contra las mujeres (tanto por parte de los hombres como de las mujeres), a la subrepresentación de las mujeres en puestos de liderazgo y prestigio, de modo que los colegas de las redes de "viejos amigos" son recomendados preferentemente para ascensos y premios, y a la baja autoestima entre las mujeres, como resultado de prejuicios culturales profundos y de larga data. Steitz ha trabajado eficazmente para contrarrestar la discriminación basada en el género, hablando para intervenir en casos individuales de discriminación, describiendo las dificultades que enfrentan las mujeres y articulando formas de superarlas.
Fuente bibliográfica
Unveiling the RNA World
Judy Lieberman, M.D., Ph.D.
Program in Cellular and Molecular Medicine, Boston Children’s Hospital, and the Department of Pediatrics, Harvard Medical School.
DOI: 10.1056/NEJMcibr1808725