Anticuerpos antiidiotípicos y SARS-CoV-2
Se plantea la hipótesis de que las respuestas inmunitarias antiidiotípicas generarían eventos adversos raros, como miocarditis, después de la vacunación contra SARS-CoV-2, así como a secuelas de la Covid-19 que persisten después de la resolución de la infección.
La investigación básica se ha centrado en destacar el trabajo de laboratorio que podría conducir a avances en la terapéutica clínica. Sin embargo, el camino es en ambos sentidos: las observaciones clínicas también plantean nuevas preguntas para los ensayos que luego conducen a la clínica. Aquí se presenta uno de una serie de artículos ocasionales que llaman la atención sobre el flujo de información.
La patogenia del síndrome respiratorio agudo severo de la infección por coronavirus 2 (SARS-CoV-2) aún no se comprende completamente, con sus efectos en múltiples sistemas orgánicos y el síndrome de "Covid prolongado" que ocurre bastante después remitir la infección. El desarrollo de vacunas ha sido fundamental para controlar la pandemia, pero la eficacia se ha visto limitada por la aparición de variantes virales, y la vacunación podría estar asociada con efectos tóxicos, incluyendo reacciones alérgicas, miocarditis, y trombosis y trombocitopenia inmunomediadas en algunos adultos sanos. Es probable que estos fenómenos estén mediados por la inmunidad. ¿Cómo podemos entender esta diversidad en las respuestas inmunes?
Una forma de pensar acerca de la complejidad es a través del lente de las reacciones antiidiotípicas. La Hipótesis de la Red, formulada en 1974 por Niels Jerne, describió un mecanismo por el cual las respuestas de anticuerpos a un antígeno inducían por sí mismas respuestas de anticuerpos posteriores contra el anticuerpo específico del antígeno. Cada anticuerpo inducido y que es específico para un antígeno (anticuerpo "Ab1") tiene regiones inmunogénicas, particularmente en sus dominios de unión al antígeno de región variable, que son únicos como resultado de la recombinación genética de los segmentos variable, de diversidad y de unión (VDJ) de la inmunoglobulina. La recombinación de VDJ da como resultado secuencias de aminoácidos nuevas y, por lo tanto, inmunogénicas llamadas idiotopos, que luego son capaces de inducir anticuerpos propios contra Ab1 como una forma de regulación negativa. Se ha propuesto un paradigma similar para las células T. Sin embargo, estas respuestas inmunitarias reguladoras también son capaces de hacer mucho más. Los paratopos, o dominios de unión a antígenos, de algunos de los anticuerpos anti-idiotipo (o "Ab2") resultantes que son específicos para Ab1 pueden parecerse estructuralmente a los de los propios antígenos originales. Por tanto, la región de unión al antígeno Ab2 representa potencialmente una imagen especular exacta del antígeno diana inicial en la respuesta Ab1, e incluso se han examinado los anticuerpos Ab2 para su potencial uso como sustituto del antígeno en los estudios de vacunas. Sin embargo, como resultado de este mimetismo, los anticuerpos Ab2 también tienen el potencial de unirse al mismo receptor al que se dirigía el antígeno original (figura 1). Los anticuerpos Ab2 que se unen al receptor original en las células normales, por lo tanto, poseen el potencial de mediar efectos celulares profundos que generarían cambios patológicos, particularmente a largo plazo, mucho después de que el antígeno original haya desaparecido.
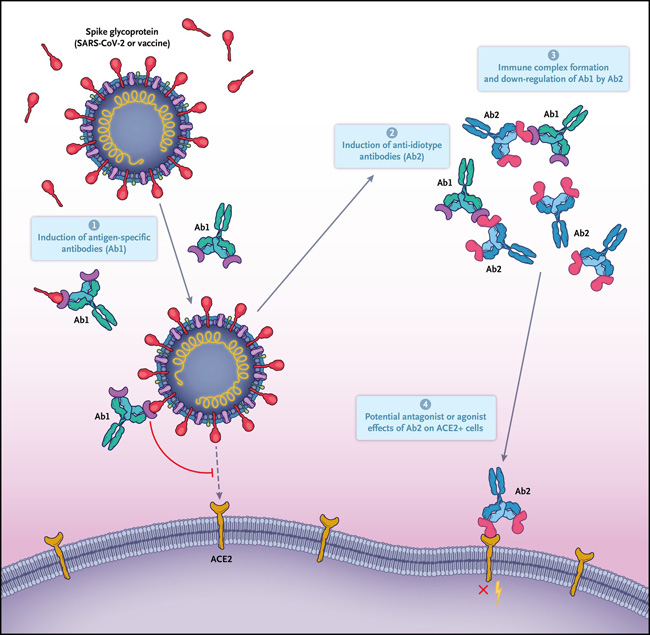
Figura 1: anticuerpos antiidiotípicos y SARS-CoV-2.
Tanto la infección por coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) como las vacunas contra él provocan anticuerpos frente a la proteína spike que el virus usa para unirse al receptor de la enzima convertidora de angiotensina 2 (ACE2) en las células diana. Estos anticuerpos se denominan Ab1. Las porciones de idiotipo de Ab1 que se unen y neutralizan la proteína spike tienen secuencias distintivas en la región determinante de complementariedad 3 (CDR3), y esas regiones de unión de anticuerpos pueden provocar por sí mismas respuestas llamadas anticuerpos antiidiotipo (Ab2) como un medio de reducción de regulación. Los anticuerpos Ab2 actuan de varias formas, como unirse al anticuerpo neutralizante protector Ab1, dando como resultado la formación y el aclaramiento de complejos inmunitarios, lo que perjudica la eficacia de Ab1. Algunas de las regiones de unión de Ab2, o paratopos, también pueden unirse al mismo objetivo que la proteína spike, el receptor ACE2. Esa unión ejercería, en teoría, varios efectos, pero no necesariamente mutuamente excluyentes, en la célula, dependiendo de la naturaleza de los anticuerpos Ab2 y el papel de los receptores celulares, por ejemplo, podría bloquear la función de ACE2 al inhibir competitivamente las interacciones normales del ligando. Alternativamente, estimularía la función de ACE2 activando el receptor, afectar la expresión de ACE2 después de unirse y regular negativamente.
Este aspecto de la regulación de las respuestas de las células inmunes fue postulado por Plotz en 1983 como una posible causa de autoinmunidad que surge después de una infección viral y desde entonces ha sido respaldado experimentalmente por la transferencia directa de anticuerpos anti-idiotipo. Los anticuerpos Ab2 generados contra el enterovirus coxsackievirus B3 en ratones pueden unirse a antígenos de miocitos, lo que resulta en miocarditis autoinmune, y las respuestas antiidiotípicas actúan como agonistas del receptor de acetilcolina, lo que lleva a síntomas de miastenia gravis en conejos. Además, al mostrar la imagen especular del antígeno viral, el Ab2 imitaría los efectos deletéreos de la propia partícula del virus, como se ha demostrado con el antígeno del virus de la diarrea viral bovina.
En la infección por SARS-CoV-2, la atención se centra en la proteína spike (S) y su uso crítico del receptor de la enzima convertidora de angiotensina 2 (ACE2) para ingresar a la célula. Dado su papel fundamental en la regulación de las respuestas de angiotensina, muchos efectos fisiológicos son influidos por la participación de ACE2. La proteína S en sí tiene un efecto directo sobre la supresión de la señalización de ACE2 mediante una variedad de mecanismos y también activa directamente los receptores tipo toll e induce citocinas inflamatorias. Las respuestas anti-idiotipo afectarían la función de ACE2, con efectos similares. Sin embargo, las evaluaciones preclínicas y clínicas de las respuestas de anticuerpos a las vacunas contra el SARS-CoV-2 se han centrado únicamente en las respuestas de Ab1 y la eficacia neutralizadora del virus. La delimitación de posibles respuestas antiidiotípicas tiene dificultades inherentes debido a su naturaleza policlonal, la cinética dinámica y la presencia concurrente de anticuerpos Ab1 y Ab2. Además, la expresión de ACE2 dentro de células y tejidos es variable. También es probable que las diferentes vacunas (ARN, ADN, adenovirus y proteína) tengan efectos diferenciales en la inducción de Ab2 o en la mediación de los efectos de la vacuna que difieren de las respuestas a la infección. Es posible que algunos efectos no deseados no estén directamente relacionados con las respuestas de Ab2. La asociación de eventos trombóticos con algunas vacunas contra el SARS-CoV-2 en mujeres jóvenes y la función etiológica de los anticuerpos anti-factor plaquetario 4-polianión puede ser el resultado del vector adenoviral. Sin embargo, la ocurrencia informada de miocarditis después de la administración de la vacuna tiene similitudes sorprendentes con la miocarditis asociada con los anticuerpos Ab2 inducidos después de algunas infecciones virales. Los anticuerpos Ab2 también podrían mediar los efectos neurológicos de la infección o las vacunas del SARS-CoV-2, dada la expresión de ACE2 en tejidos neuronales, los resultados neuropatológicos específicos de la infección por SARS-CoV-2 y la similitud de estos con los efectos neurológicos mediados por Ab2 observados en otros modelos virales.
Por lo tanto, sería prudente caracterizar completamente todas las respuestas de anticuerpos y células T al virus y las vacunas, incluidas las respuestas de Ab2 a lo largo del tiempo. Usar ratones transgénicos huACE2 y cruzarlos con cepas que están predispuestas a la autoinmunidad u otras condiciones patológicas humanas podría proporcionar información importante. La comprensión de las posibles respuestas de Ab2 daría información sobre el mantenimiento y la eficacia de Ab1, y sobre la aplicación de agentes terapéuticos basados en anticuerpos. Sin embargo, se necesita mucha más investigación científica básica para determinar el potencial impacto que desempeñaría la inmunorregulación basada en idiotipos de las respuestas humorales y mediadas por células, tanto en la eficacia antiviral como en los efectos secundarios no deseados de la infección por SARS-CoV-2 y de las vacunas.
Fuente bibliográfica
Basic Implications of Clinical Observations: A Possible Role for Anti-idiotype Antibodies in SARS-CoV-2 Infection and Vaccination
William J. Murphy, Ph.D. and Dan L. Longo, M.D.
Departments of Dermatology and Internal Medicine, Division of Hematology and Oncology, University of California, Davis, Sacramento (W.J.M.).
DOI: 10.1056/NEJMcibr2113694