Actualización epidemiológica en SARS-CoV-2
A fines de diciembre de 2019, se informó en Wuhan (China) de un grupo de pacientes con "neumonía atípica" de etiología desconocida. Un nuevo coronavirus humano, llamado provisionalmente SARS-CoV-2, fue identificado como la causa de esta enfermedad, ahora denominada COVID-19. Cada vez se reconoce más que los coronavirus pueden ser los agentes etiológicos de importantes amenazas emergentes para la salud humana, siendo los síndromes respiratorios SARS y MERS dos ejemplos recientes, mientras que dos coronavirus ahora endémicos en humanos (229E y OC43), han surgido de animales en los últimos cientos de años. El brote de SARS-CoV-2 comenzó en diciembre de 2019 y al 30 de enero de 2020, la Organización Mundial de la Salud declaró este evento como una emergencia de salud pública de interés internacional. Múltiples publicaciones tratan de describir el escenario epidemiológico actual, las que en un intento coordinado a nivel global destacan algunos de los principales hallazgos relacionados con esta epidemia.
Conocimiento viral en expansión
El SARS-CoV-2 puede cultivarse fácilmente a partir de muestras clínicas, y los aislados virales ya están disponibles en China continental y en otros lugares del mundo. El SARS-CoV-2 es genéticamente similar a otros coronavirus del subgénero Sarbecovirus, un clado de betacoronavirus formado por el ejemplar que causa el SARS (SARS-CoV) y otros similares que se encuentran en murciélagos. Las recombinaciones entre coronavirus son comunes y se cree que el SARS-CoV es una recombinación entre los sarbecorvirus de los murciélagos. Curiosamente, todo el genoma del SARS-CoV-2 es muy similar al de un coronavirus de murciélago detectado en 2013 (>96% de identidad de secuencia) lo que sugiere que el antepasado inmediato del SARS-CoV-2 ha estado circulando en murciélagos durante al menos varios años.
Los análisis completos del genoma del virus indican que esta epidemia fue causada por una única introducción zoonótica y que el virus es genéticamente estable en humanos. El primer grupo se notificó en asociación con la exposición a un mercado de mariscos que se sabe que vende animales vivos de caza silvestres para el consumo. Es posible que la transmisión zoonótica del SARS-CoV-2 implique un hospedero intermediario (o varios), como se observó en la epidemia de SARS. Sin embargo, algunos de los primeros casos no tuvieron exposición epidemiológica a este mercado. Por consiguiente, todavía no está claro si el salto zoonótico inicial se produjo directamente de los murciélagos a los humanos o si estuvo involucrada otra especie de mamíferos como intermediario. La identificación del reservorio precedente es pertinente porque es muy posible que se produzcan nuevos episodios de transmisión zoonótica a menos que se identifiquen e interrumpan las vías de transmisión del episodio zoonótico inicial.
Investigaciones anteriores sobre varios coronavirus de murciélago similares al SARS-CoV demostraron que algunos de estos virus pueden utilizar como receptor a la enzima convertidora de angiotensina tipo 2 (ECA-2) humana para la infección. La glucoproteína S del SARS-CoV-2, que se proyecta como espículas desde la superficie de la particular viral, es estructuralmente similar a la del SARS-CoV (DOI: 10.1016/S0140-6736(20)30251-8) y, de hecho, puede ser blanco de un anticuerpo monoclonal que es específico para la espícula del SARS-CoV (DOI: 10.1080/22221751.2020.1729069). Aunque en la espícula del SARS-CoV-2 se encontraron variaciones en residuos aminoacídicos clave que son esenciales para la unión a ECA-2, este nuevo virus es capaz de utilizar ECA-2 de humanos, cerdos, murciélagos y civeta, pero no la de ratones, para su entrada. La proteína de espícula del SARS-CoV-2 también puede interactuar teóricamente con ECA-2 de otras especies animales (DOI: 10.1128/JVI.00127-20).
Clínica de la enfermedad por SARS-CoV-2
En los informes clínicos iniciales de 99 pacientes en los que se confirmó infección con SARS-CoV-2, se observaron comúnmente síntomas de fiebre y tos (>80%). También se evidenció falta de aliento (31%) y dolores musculares (11%). En contraste con los infectados por coronavirus humanos que causan el resfriado común, el escurrimiento nasal y el dolor de garganta fueron menos comunes (≤5%) en los hospitalizados, pero pueden ser más frecuentes en enfermedades leves (DOI: 10.1056/NEJMc2001468). En serie de casos hospitalarios se han observado pruebas radiológicas de neumonía bilateral (75%) o unilateral (25%), a veces con indicios de múltiples opacidades moteadas y de vidrio esmerilado. El 17% de los pacientes desarrollaron el síndrome de dificultad respiratoria aguda que a veces daba lugar a la disfunción de múltiples órganos y a la muerte. Aproximadamente el 75% de los afectados requirió oxígeno suplementario, y el 13%, ventilación mecánica. La edad de los sujetos afectados osciló entre los 21 y los 82 años, con el 67% de ellos con más de 50 años y el 51% con comorbilidades subyacentes. Las presentaciones clínicas y la progresión fueron ampliamente similares a las de los pacientes con MERS o SARS (DOI: 10.1016/S0140-6736(20)30211-7).
Datos recientes de grupos de casos sugieren que el espectro clínico general de esta enfermedad puede ser más heterogéneo (DOI: 10.1016/S0140-6736(20)30154-9). Los síntomas de las vías respiratorias superiores como el dolor de garganta y congestión nasal, así como la diarrea, pueden verse en casos más leves. La evidencia radiológica de neumonía puede verse incluso en infecciones asintomáticas. Estos grupos de pacientes también sugieren que la edad avanzada se asocia con enfermedades más graves, y que los adultos jóvenes y niños tienen enfermedades progresivamente menos graves. También se observó en el SARS un aumento de la gravedad de la enfermedad asociado a la edad.
Las muestras de las vías respiratorias inferiores (por ejemplo, esputo) parecen tener una carga viral más alta que las de las superiores (por ejemplo, frotis de garganta). También se detectó ARN viral en muestras de sangre y heces (DOI: DOI: 10.1056/NEJMoa2001191), pero se desconoce si estas muestras no respiratorias son infecciosas. Dado que las muestras fecales de pacientes con SARS eran infecciosas en algunos casos (por ejemplo, el incidente de Amoy Gardens en Hong Kong), es aconsejable tomar precauciones contra la transmisión fecal oral.
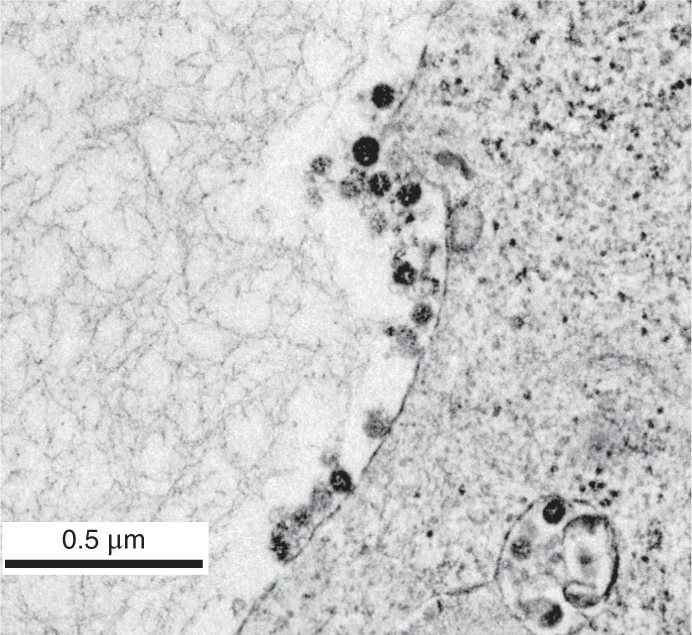
Figura 1. Microscopía electrónica que muestra el SARS-CoV-2 aislado en la Universidad de Hong Kong. Proporcionado por John Nicholls (Departamento de Patología).
Aparte de los primeros casos (DOI: 10.1056/NEJMoa2001316) las infecciones humanas posteriores fueron causadas por una transmisión sostenible de persona a persona. Utilizando los primeros 425 casos confirmados en Wuhan, Qun Li y colaboradores estimaron que el período medio de incubación del SARS-CoV-2 era de 5,2 días (IC del 95%, 4,1 - 7,0), y que alrededor de 95% de los casos desarrollaron síntomas dentro de los 12,5 días tras una exposición, lo que justifica las recomendaciones actuales de un período de 14 días para la observación médica o la cuarentena. El número reproductivo (R0; número de casos secundarios esperados en una población completamente susceptible) y el tiempo de duplicación de la epidemia, se estimaron en 2,2 (IC 95%, 1,4 - 3,9) y 7,4 días (IC 95%, 4,2 - 14), respectivamente. Otros estudios también han dado lugar a cifras muy similares (DOI: 10.1016/S0140-6736(20)30260-9). Éstas son comparables a las observadas durante la epidemia de SARS. Sin embargo, la transmisión del SARS-CoV-2 puede ocurrir en pacientes con una enfermedad leve, aunque sigue siendo controversial si la transmisión se produce durante el período de incubación tardía. Esto contrasta fuertemente con el patrón de transmisión observado durante el SARS, para el cual la transmisión rara vez se produjo hasta después de los 4 o 5 días posteriores a la aparición de los síntomas. En conjunto, estas conclusiones sugieren que es poco probable que las intervenciones de salud pública que interrumpieron con éxito la propagación del virus del SARS sean tan eficaces en el brote actual.
Utilizando los datos del número de casos exportados de Wuhan y los datos sobre las pautas de viaje, Wu y colaboradores estimaron que había >75.000 personas infectadas en Wuhan entre el 1 de diciembre de 2019 y el 25 de enero de 2020 (DOI: 10.1016/S0140-6736(20)30260-9). Con las tendencias actuales y suponiendo una reducción de la transmisibilidad debido a las intervenciones, predijeron que el brote en Wuhan alcanzaría su punto máximo en abril de 2020. También predijeron que esta epidemia seguirá creciendo exponencialmente fuera de Wuhan. Sus simulaciones sugirieron además que una reducción de 50% en la transmisión de esta enfermedad lograda a través de intervenciones de salud pública, pero sin una reducción en el movimiento de la población, puede retrasar dramáticamente el crecimiento exponencial de esta enfermedad por lo menos unos meses. Si bien la aplicación de medidas agresivas de control de la patología, como el cierre de escuelas y el distanciamiento social, puede retrasar el establecimiento de la transmisión en los países con riesgo de importación de casos, todavía no está claro si se puede prevenir la propagación mundial de esta enfermedad.
Aunque se ha aprendido mucho en las últimas semanas, sigue habiendo una serie de lagunas de conocimiento cruciales. Entre ellas se encuentran los modos de transmisión, la estabilidad del virus en los entornos, los mecanismos de patogénesis y cuáles son los tratamientos y vacunas eficaces. En las circunstancias actuales, la cuestión más importante es la severidad de la enfermedad. Cabe señalar que en la etapa inicial de la pandemia del virus de la gripe H1N1 de 2009 se notificaron estimaciones de casos fatales de hasta 10%. Sin embargo, los estudios seroepidemiológicos estratificados por edad basados en la población, revelaron que la verdadera letalidad general de este brote de influenza era de alrededor del 0,001% (DOI: 10.1097/EDE.0b013e3182a67448). Por lo tanto, la seroepidemiología es necesaria para una estimación fiable de la verdadera gravedad de la enfermedad. Las infecciones pasadas también pueden traducirse en la inmunidad de la población, que son datos que deben tenerse en cuenta en los futuros modelos de transmisión del virus. Es relevante señalar también que la infección por MERS-CoV o la enfermedad subyacente no siempre conducen a respuestas detectables de anticuerpos (DOI: 10.3201/eid2307.170310). Si la infección del SARS-CoV-2 tiene una cinética de respuesta de anticuerpos similar a la de la infección por MERS-CoV, esto puede tener implicaciones para la seroepidemiología y el desarrollo de la inmunidad de rebaño. Por lo tanto, es prioritario investigar la cinética de respuesta humoral y además la celular para tener una comprensión más acabada sobre el SARS-CoV-2.
Fuente bibliográfica
Emergence of a novel human coronavirus threatening human health
Leo L. M. Poon & Malik Peiris
School of Public Health, LKS Faculty of Medicine, The University of Hong Kong, Hong Kong, China
DOI: 10.1038/s41591-020-0796-5