Delta-FosB
La esencia de la depresión
Hace algunos años, los científicos habían creído encontrar una clave sobre la adicción a la cocaína, permitiendo pensar en futuros tratamientos más eficaces. Lo importante es que era una proteína que funcionaba casi como un "interruptor" capaz de habilitar el incontrolable antojo de los toxicómanos. A tal molécula de interés se le llamó delta-FosB, un factor de la transcripción. Los investigadores saben desde hace algún tiempo de que el uso prolongado de cocaína aumenta la producción de esta proteína en el núcleo accumbens, una región del cerebro importante para la percepción del placer. Los estudios pusieron de manifiesto que el uso prolongado de cocaína, anfetaminas, morfina y nicotina desencadenaba la producción de delta-FosB, ésta, entonces, activaba un gen productor de los componentes de diversos neurotransmisores, como la dopamina y serotonina. Además, ya hay cierta evidencia que delta-FosB causa cambios estructurales dentro de los accumbens nucleares, que ayuda probablemente a perpetuar los cravings, y puede ser responsable de la alta incidencia de recaídas que ocurren en drogadictos tratados.
Ahora, y de acuerdo con un nuevo estudio en ratones, esta proteína en el cerebro parece ejercer una influencia significativa en los sentimientos de desesperación. Los roedores que tienen niveles más elevados de delta-FosB enfrentaron mejor los retos frustrantes presentados en el experimento. Los investigadores especulan que la proteína también podría ayudar al cerebro humano a controlar mejor las situaciones estresantes.
Por otra parte, la sustancia P es uno de las varias docenas de neurotransmisores conocidos, muy abundante en el cerebro de los mamíferos. Es un péptido de cadena corta identificado hace casi 80 años pero que, a pesar de su larga vida como molécula bien identificada, se ha resistido a desvelar sus secretos, especialmente por lo que se refiere a su participación en la percepción del dolor. Desde hace tiempo se sabe que participa de alguna manera en las señales que el sistema nervioso requiere para percibir el dolor, también que es esencial para el desarrollo de los primeros pasos de las reacciones inflamatorias, especialmente de las que se originan como consecuencia de heridas o lesiones de la piel, pero su mecanismo de acción preciso y sus funciones generales en el sistema nervioso quedan por desvelarse.
Finalmente, las recientes investigaciones han establecido interacciones entre estas dos moléculas, ya que se ha observado que los niveles crecientes de delta-FosB disminuyen la actividad del gen que codifica para la sustancia P, reguladora de procesos tales como el ánimo, sensibilidad del dolor, ansiedad y estrés. Estos resultados proporcionan notables fundamentos y un modelo reproducible para evaluar los mecanismos de la resistencia. Próximos estudios probarán la hipótesis que los tratamientos antidepresivos pueden realzar la resistencia al estimular estos mismos procesos adaptativos, que ocurren espontáneamente sólo en algunos individuos de una población expuesta al estrés crónico.
Moléculas que regulan el estado de ánimo
Al trastorno depresivo mayor se le reconoce como uno de los grandes problemas de salud pública a nivel mundial: es frecuente, por lo general, sigue un curso de recaídas o recurrencias, perturba el desempeño de las funciones sociales y profesionales, y está asociado con una mayor morbilidad médica y una reducción de la esperanza de vida. Durante las últimas décadas, los antidepresivos se han convertido en el medio más utilizado para disminuir el sufrimiento y los perjuicios asociados con esta heterogénea enfermedad.
Los medicamentos más nuevos, como los inhibidores selectivos de la recaptación de serotonina y norepinefrina, han mejorado los resultados en comparación a los principios tricíclicos, en términos de efectos secundarios, la facilidad de uso y la disminución de la letalidad en caso de sobredosis. Sin embargo, estas nuevas terapias de primera y segunda línea todavía tienen limitaciones claras, y menos del 50% de los pacientes que han comenzado el tratamiento estará en condiciones relativamente favorables un año más tarde.
La identificación de nuevos antidepresivos que puedan ampliar la eficacia o incluso mejorar el perfil de tolerabilidad, sigue siendo una importante área de investigación. Dado que el campo puede estar acercándose a un punto de rendimiento decreciente con respecto a nuevos medicamentos que bloqueen los transportadores de la serotonina y norepinefrina, la atención se desplaza a otros mecanismos que sean capaces de regular los cambios de los eventos implicados en las neuronas y en la genómica en respuesta a los antidepresivos.
Por lo tanto, un reciente estudio de Olivier Berton y colegas (Neuron. 2007 Jul 19; 55(2):289-300) es de gran interés para los neurólogos, médicos y las personas con depresión y sus seres queridos. Resumiendo brevemente, los investigadores han estudiado la correlación molecular del “desamparo aprendido”, uno de los mejores modelos animales validados para la depresión humana. El desamparo aprendido es un estado de déficit de comportamiento que es inducido experimentalmente por la colocación de animales de laboratorio en una situación en la que es imposible escapar a la estimulación aversiva, en el tiempo que los animales aprenden a "reducir sus pérdidas" por la adopción de un comportamiento pasivo, que característicamente persiste durante algún tiempo después del cambio de situación y entonces el escape podría ser posible. Hay diferencias que son específicas de las especies y poblaciones para el desarrollo del desamparo aprendido, así como diferencias individuales dentro de las mismas especies y cepas. Algunos animales son más resistentes (siguen intentando escapar) o resilentes (ellos continúan tratando de huir o permanecen inermes por un corto tiempo para después intentar escapar si es posible).
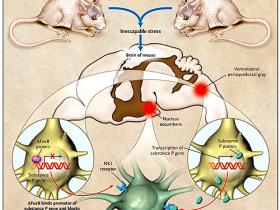
Anteriores investigaciones habían demostrado que el desamparo aprendido está asociado con la inducción del factor de transcripción delta-FosB en varias regiones del cerebro, incluyendo el núcleo dorsal del rafe (principal fuente cerebral de serotonina), el locus ceruleus (principal fuente de norepinefrina en el cerebro) y la sustancia gris ventrolateral periacueductal, una región esencial para la percepción del dolor y un sitio rico en neuronas que contienen el neurotransmisor neuropéptido sustancia P, agonista endógeno de los receptores de la neuroquinina-1.
Berton y colegas, han encontrado que los niveles de delta-FosB predicen fuertemente las diferencias individuales en magnitud del comportamiento frente a un trauma inevitable. Concretamente, los animales con mejor respuesta a delta-FosB en la sustancia gris ventrolateral periacueductal son los más resistentes o resilentes a las consecuencias del comportamiento de desamparo aprendido. Esta asociación es tan fuerte (r = 0.69) que uno podría suponer que la mitad de la diferencia de comportamiento podría explicarse por la inducción de la expresión de delta-FosB.
Los investigadores, además, encontraron que la inducción de delta FosB predomina en las neuronas con tinción positiva de la sustancia P, y que el gen que codifica dicha molécula es regulado por delta-FosB (Figura 1). Para probar si la modulación de delta-FosB sobre la sustancia P en neuronas de la sustancia gris ventrolateral periacueductal influye en la neurotransmisión de la sustancia P, los autores diseñaron ratones que sobre-expresaban delta-FosB, a través de un plásmido inactivo que contenía beta-galactosidasa o LacZ (como forma de control), y midieron la liberación de la sustancia P en el núcleo accumbens, tanto bajo condiciones basales como después de la exposición al estrés. El núcleo accumbens, que se une con el tubérculo olfativo para compensar el cuerpo estriado ventral, desempeña una función fundamental en el apetito y en otros comportamientos de recompensa y, por consiguiente, está directamente implicado en la mediación de algunas deficiencias de comportamiento de la depresión en seres humanos. A pesar de que la sobre-expresión de delta-FosB no cambió significativamente las concentraciones extracelulares de referencia de la sustancia P en el núcleo accumbens, sí reprimió significativamente un aumento de los niveles de la sustancia P, en respuesta a dos técnicas de laboratorio estandarizadas para el estrés. Los investigadores observaron efectos similares en la administración del antidepresivo tricíclico desipramina, con el fin de calibrar el resultado relativo de un fármaco que ha demostrado invertir el desamparo, y ser un antagonista específico del receptor de la neuroquinina-1, bloqueando la disminución de la sustancia P (en este caso, obstaculizando la potenciación de las neuronas inhibidas por el ácido gamma-aminobutírico [GABA] en el núcleo accumbens, pudiendo mediar por lo menos algunos de los déficit de comportamiento del estado de desamparo aprendido).
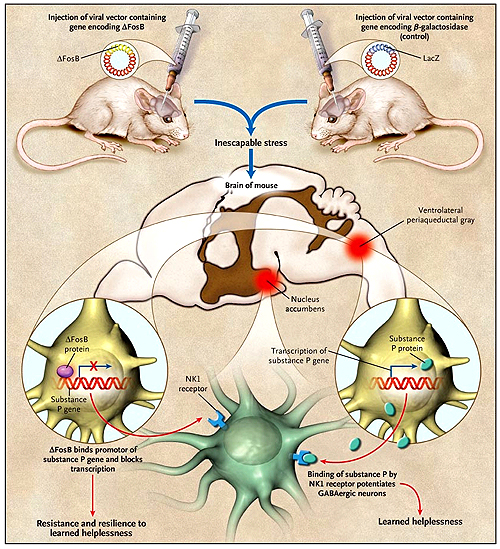
La inyección de un vector viral en un ratón altera los neuroquímicos del animal y las respuestas de comportamiento al estrés ineludible. Entonces, la inhibición de la síntesis de la sustancia P por delta-FosB en la región gris ventrolateral periacueductal reduce la inhibición del comportamiento de escape a través del ácido gamma-aminobutírico (GABA) en el núcleo accumbens. NK1 denota a la neuroquinina-1.
No cabe duda de que los nuevos antidepresivos han mejorado el desempeño a través de mecanismos diferentes a la inhibición de los transportadores de la serotonina y norepinefrina generando valor agregado para la comunidad médica. Un gran salto de fe y mucho trabajo son necesarios para completar estos experimentos y la introducción de un tratamiento seguro para las personas con una depresión compleja y heterogénea. No obstante, las conclusiones de Berton y colaboradores, avanzan con respecto a la aclaración de la base neural de las diferencias individuales de respuestas de comportamiento al estrés sostenido. En este sentido, los experimentos identifican a delta-FosB como un importante mediador de las respuestas de comportamiento, han localizado la región de mayor interés en la sustancia gris ventrolateral periacueductal y han puesto de relieve la pertinencia de la sustancia P como un objetivo para la intervención farmacológica. La conclusión de que la sobre-expresión de delta-FosB cambia el fenotipo del comportamiento (de estrés sensible a estrés resistente) puede proporcionar una visión de futuras estrategias psicofarmacológicas, en particular si tales manipulaciones tienen efectos fenotípicos duraderos. El hecho de que los estudios clínicos aún no han confirmado un efecto antidepresivo consistente para los antagonistas específicos de los receptores de la neuroquinina-1 puede potenciar los esfuerzos en tratamientos que directamente se centren en los mecanismos intracelulares, como la actividad de delta-FosB.
Fuente bibliográfica
Molecules That Mediate Mood
Michael E. Thase, M.D.
University of Pennsylvania School of Medicine and the Veterans Affairs Medical Center, Philadelphia, USA.
N Engl J Med. 2007 Dec 6;357(23):2400-2