Nanopartículas e inmunoterapia contra el cáncer
La resistencia a un inhibidor de control inmunitario es un obstáculo importante para este tipo de terapia.
La respuesta inmune frente al cáncer envuelve una serie de eventos espaciotemporales que son definidos bajo el paraguas del "Ciclo Inmune del Cáncer" y se inicia con la detección innata de células cancerosas por parte de las células dendríticas (CD).
El estimulador del gen del interferón (de su nombre en inglés Stimulator of interferon genes, STING) parece ser indispensable para esta detección. La vía STING reconoce el ADN citosólico y el dinucleótido cíclico (DNC), lo que lleva a la inducción de interferones tipo I (IFN) y la producción de citoquinas inflamatorias asociadas con la inmunidad innata. Por lo tanto, los agonistas asociados a la vía de STING, como los ADN y los DNC, podrían actuar como potentes adyuvantes contra el cáncer.
El avance de la inmunoterapia contra el cáncer liderado por el éxito de los inhibidores de puntos de control inmunitarios (ICI), está lejos de detenerse. Sin embargo, sólo una pequeña parte de los pacientes pueden recibir los beneficios de los ICI y una gran parte no responden a los ICI. La resistencia a los ICI, especialmente a los anti-PD- 1/ PD-L1, es un obstáculo importante en el estado actual de la inmunoterapia contra el cáncer. Informes recientes han revelado que las células depredadoras naturales (del inglés natural killers NK) activadas por la estimulación de la vía STING pueden tener efectos prometedores en las respuestas antitumorales.
Investigadores de la Facultad de Ciencias Farmacéuticas de la Universidad Hokkaido en Japón, lograron demostrar que si bien, la monoterapia anti-PD- 1 no logró inducir un efecto antitumoral, la combinación del STING-LNP y el anti-PD- 1 ejerció un efecto sinérgico. Sus resultados indicaron que el tratamiento con STING-LNP aumentó significativamente la expresión de CD3, CD4, NK1.1, PD-1 y el interferón (IFN)-γ en las metástasis de pulmón.
En conclusión, un tratamiento con STING-LNP puede superar la resistencia a PD-1 en un modelo de metástasis pulmonar. El mecanismo responsable de esto indica que las células depredadoras naturales (NK) son activadas estimulando la vía STING que, a su vez, induce la expresión de PD-L1 en las células cancerosas. En base a los hallazgos, el STING-LNP representa un prometedor candidato para su uso en la terapia combinada con tumores resistentes al anti-PD-1.
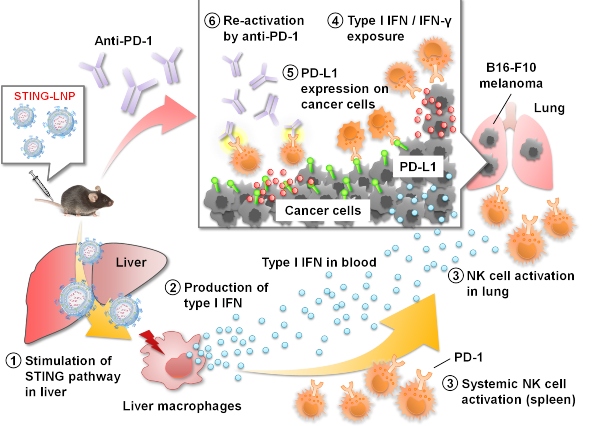
Resumen de la reducción de la resistencia a los anti-PD-1 por STING-LNP.








