Nefrología
Proteinuria e inmunidad: ¿relación exagerada?
El glomérulo renal es una estructura altamente especializada que garantiza la ultrafiltración selectiva del plasma a fin de que las proteínas esenciales se conserven en la sangre. El denominador común en una variedad de enfermedades renales, incluida la enfermedad de cambio mínimo y glomerulosclerosis segmentaria focal, es la disfunción del podocito que involucra una pérdida masiva de proteínas en la orina (proteinuria). La dinámica de la regulación del citoesqueleto de actina en los podocitos es vital para la normal función filtradora de los riñones, y las mutaciones que afectan a las proteínas del podocito conducen a la reorganización del citoesqueleto de actina y a la posterior proteinuria. Estas proteínas del citoesqueleto que regulan la dinámica de la actina, por lo tanto, son cruciales para mantener la función glomerular.
Por ejemplo, la sinaptopodina (proteína de unión a actina: actin-binding protein) es una de las unidades importantes de los podocitos y una parte del aparato contráctil basado en los procesos pediculados. La proteína de 100-kDa participa activamente en la integridad de la barrera de filtración glomerular, pero también se expresa en el cerebro y en la columna vertebral, a través de un subconjunto de neuronas telencefálicas.
Ciclosporina y el podocito
La proteinuria es un signo importante de la enfermedad renal, un marcador, y un factor de riesgo independiente para la patología cardiovascular. Es la primera señal de complicaciones renales de la diabetes, la obesidad y el síndrome metabólico. Por lo tanto, terapias para reducirla o prevenirla, son altamente deseables. Varios adelantos han contribuido a perfeccionar los objetivos para su manejo, y - como el reciente estudio realizado por Christian Faul y colegas (Nat Med 2008; 14:931-938) muestra - estos avances han generado algunas sorpresas.
La proteinuria se produce cuando aumenta la permeabilidad de la capilaridad glomerular. Este incremento puede producirse a causa de lesiones inflamatorias provocadas por enfermedades autoinmunes sistémicas como el lupus o la vasculitis de vasos pequeños. En estas situaciones, es fácil comprender por qué los agentes antiinflamatorios como los corticosteroides o los inmune-moduladores como la ciclosporina o ciclofosfamida, o ambos, pueden representar tratamientos eficaces. Sin embargo, la efectividad de estos fármacos en la patología renal proteinúrica en la que no hay inflamación, como la nefropatía de cambio mínimo y la glomerulosclerosis segmentaria focal, es más difícil de explicar. Dado que los medicamentos actúan principalmente en las células del sistema inmunológico, los nefrólogos tradicionalmente han invocado sus explicaciones a partir de la relación entre los linfocitos (y los factores solubles producidos por ellos) y las lesiones renales. Sin embargo, es escasa la evidencia que apoye este tipo de vínculo.
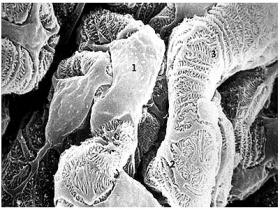
El estudio de C. Faul y colaboradores se ocupa de esta anomalía, centrándose en el podocito, una de los principales tipos celulares de la pared capilar glomerular y que prevendría la proteinuria en personas sanas. La función del podocito depende de una singular y compleja estructura (figura 1) que, a su vez, necesita de un citoesqueleto de actina muy regulado. Los autores encontraron que la ciclosporina, cuya efectividad frecuentemente ha sido descrita como prueba de un papel etiológico clave de los linfocitos T en enfermedades proteinúricas, tiene efectos directos sobre el citoesqueleto de actina y por lo tanto en la forma de los podocitos.
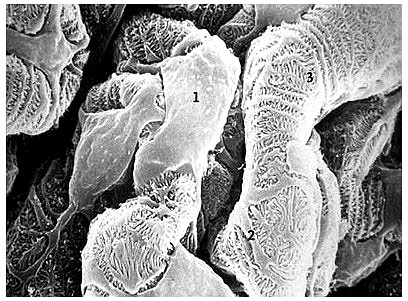
El microscopio electrónico de barrido muestra el aspecto exterior (urinario) de una pared capilar glomerular humana normal. Los podocitos tienen características morfológicas complejas con células orgánicas (1), procesos primarios (2), y procesos secundarios que se entrecruzan (3) entre sí para formar rendijas de filtración.
El mecanismo (figura 2) implica a la sinaptopodina, un estabilizador clave para los podocitos en el citoesqueleto de actina. Cuando sinaptopodina está fosforilada, se une a otra proteína llamada 14-3-3 y así se protege de la degradación. La calcineurina, que está bloqueada por la ciclosporina, desfosforila a sinaptopodina y permite su degradación. C. Faul y colaboradores también encontraron que el aumento de resistencia a la degradación en los podocitos protege contra la proteinuria y que la expresión de la calcineurina en los podocitos conduce a la proteinuria.
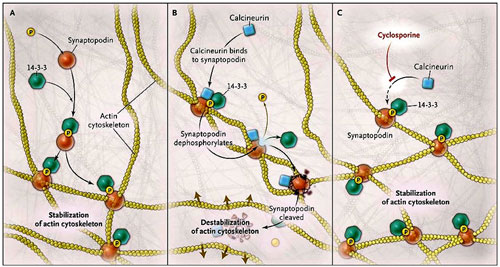
Cuando la sinaptopodina se fosforila se une a la proteína 14-3-3 y protege de la degradación. La sinaptopodina estabiliza el citoesqueleto de actina, permitiendo que el podocito mantega su forma (panel A). La calcineurina desfosforila a la sinaptopodina, la que luego se separa de 14-3-3 pudiendo ser degradada por la catepsina L. Entonces, su efecto estabilizador sobre el citoesqueleto de actina se pierde, y la célula se deforma (panel B). La ciclosporina inhibe la acción de la calcineurina, previniendo la desfosforilación de la sinaptopodina y mantiene el efecto estabilizador de la actina (panel C). P denota la fosforilación.
En conjunto, los resultados proporcionan apoyo a la afirmación de que el resultado antiproteinúrico de la ciclosporina puede explicarse por sus efectos directos sobre los podocitos y no por sus acciones sobre los linfocitos T. Esto sugiere que la nefrología ha utilizando el enfoque correcto debido a una razón equivocada, planteando la tentadora posibilidad de que otras enfermedades proteinúricas (la nefropatía diabética es el reto clínico más importante) también podrían ser tratadas por agentes que estabilizan el citoesqueleto de podocitos. Es evidente que este concepto tendrá valor práctico cuando se desarrollen agentes más selectivos; los complejos efectos de la ciclosporina incluyen la nefrotoxicidad, por lo que no parece ser una opción razonable para el tratamiento de la nefropatía diabética.
Por lo tanto, ¿el sistema inmune participa en la inducción de la proteinuria? La mayoría de las pruebas que apoyan este modelo se han basado en la eficacia del rituximab, un agente selectivo anti células B, en enfermedades proteinúricas. No obstante, los datos descritos por el grupo de C. Faul sugieren la necesidad de una evaluación de los agentes destinados a los linfocitos como elección más lógica, habida cuenta de que su eficacia podría ser, al menos en parte, explicada por los efectos directos sobre los podocitos.
Se ha planteado una sugerencia similar durante los últimos años respecto a los glucocorticosteroides en las condiciones proteinúricas: los estudios han demostrado que estos medicamentos tienen efectos sobre los podocitos, incluidos sobre el citoesqueleto de actina. P. Grimbert y colegas recalcan la tendencia entre los nefrólogos. Ellos identificaron una proteína denominada c-mip que afecta al citoesqueleto de actina en los linfocitos y que se encuentra sobre-regulada en pacientes con síndrome nefrótico. Recientemente se ha observado que la misma proteína está sobre-regulada en los podocitos de enfermedades proteinúricas, y también encontraron que la sobre-expresión específica en podocitos conduce a la proteinuria. Los podocitos sobre-expresan c-mip adquiriendo las mismas características morfológicas que la de los encontrados en enfermedades proteinúricas humanas, con fallas en los procesos y la pérdida cortical del citoesqueleto de actina. Independientemente de que c-mip sea inducida, tanto en linfocitos como podocitos, por un agente común, los resultados indican que es la anormalidad del podocito la cual debe ser objeto de terapia. Insospechadas similitudes entre el podocito y el linfocito son la base de lo que ahora parece ser un planteamiento erróneo: los ataques del sistema inmunológico.
En conjunto, estos estudios apuntan al podocito como un objetivo atractivo y, en particular, al citoesqueleto de actina, en donde, la estabilización de las características morfológicas es muy importante.
Fuente bibliográfica
Proteinuria and Immunity — An Overstated Relationship?
Peter W. Mathieson, Ph.D.
Academic Renal Unit, University of Bristol and Southmead Hospital - both in Bristol, United Kingdom.
N Engl J Med. 2008 Dec 4;359(23):2492-4