Tecnología CRISPR para la liberación de fármacos
Los materiales sensibles a los estímulos activados por señales biológicas juegan un papel cada vez más importante en las aplicaciones de la biotecnología. En ese sentido, se puede aprovechar la programabilidad de las enzimas nucleasas asociadas a CRISPR para accionar a hidrogeles que contienen ADN como elemento estructural o como anclaje de grupos suspendidos. Tras la activación mediante un ARN guía, la nucleasa Cas12a corta el ADN estructural de los geles, convirtiendo así la información biológica en cambios en las propiedades del material. Estos materiales permiten una gama de aplicaciones in vitro en ingeniería de tejidos, bioelectrónica y diagnóstico. La fabricación de diferentes tipos de hidrogeles CRISPR podrían ser potencialmente utilizados como biosensores (por ejemplo, para detectar genes de Staphylococcus aureus resistente a la meticilina o el virus del Ébola) o como sistemas de administración de fármacos y células, ofreciendo nuevas alternativas de tratamiento basadas en la liberación eficiente de agentes terapéuticos.
Biodetección
Los sistemas de administración que pueden ser activados para liberar un fármaco in situ tienen ventajas sobre los métodos convencionales de administración de fármacos y se han vuelto más deseables con el desarrollo de moléculas grandes, como los medicamentos biológicos. La biosensibilidad es fundamental para las pruebas de diagnóstico, que incluyen diagnósticos médicos en laboratorio y pruebas en puntos de atención no basados en laboratorios, que son fundamentales para gestionar la salud de las personas que viven en zonas de recursos limitados y para prevenir la propagación de enfermedades infecciosas. En relación con lo anterior, un estudio reciente llevado a cabo por English y colaboradores otorga noticias alentadoras: describen un medio para programar molecularmente materiales tradicionales de manera que puedan ser utilizados para entregar un medicamento o usarse como biosensores.
Se han desarrollado y sintetizado muchos materiales para aplicaciones médicas biológicas. Un ejemplo incipiente es el poli(ácido láctico-co-glicólico) (PLGA), un polímero biodegradable aprobado por la Administración de Alimentos y Medicamentos y la Agencia Europea de Medicamentos y que consiste en unidades repetidas de dos monómeros (ácido láctico y ácido glicólico). Se utiliza en vehículos para la administración de medicamentos. El PLGA es generalmente biocompatible, lo cual no es una sorpresa, dado que ambos monómeros son sintetizados por las células. Al igual que PLGA, el ADN también es un polímero. Es una larga cadena molecular que consiste en cuatro tipos de monómeros (los nucleótidos adenosina, timina, citosina y guanina) y puede utilizarse como vehículo de administración. De hecho, utilizando sólo el ADN como polímero, los científicos han fabricado hidrogeles para la entrega de medicamentos y la producción de proteínas libre de células (DOI: 10.1021/acs.accounts.6b00581).
Cuando se combina con las enzimas, el ADN tiene funciones impresionantes. El sistema de repeticiones palindrómicas cortas agrupadas y regularmente interespaciadas (CRISPR) es especialmente potente. El sistema CRISPR más utilizado se llama CRISPR-Cas9, en el que la enzima Cas9 (una endonucleasa) corta el ADN de doble cadena en un sitio específico: la ubicación del sitio de corte se determina por la secuencia del ARN guía, llamado así porque guía a la endonucleasa Cas9 hacia la secuencia de ADN que es complementaria al ARN guía (figura 1). Una vez que se une al ADN de doble hebra, la enzima se activa y rompe el ADN. Este es el primer paso para modificar o eliminar un gen (es decir, la edición del gen). El sistema CRISPR ha sido ampliado con el descubrimiento e incorporación de Cas12a, una endonucleasa similar a la Cas9. Al igual que la Cas9 activada, la Cas12a activada corta el ADN de doble hebra, pero a diferencia de la Cas9, se activa y desencadena un frenesí de ruptura indiscriminada del ADN monocatenario (a una tasa de aproximadamente 1.200 cortes por segundo), causando daños colaterales. Es este sistema -CRISPR-Cas12a- el que English y sus colaboradores utilizaron para crear nuevos materiales para la administración de medicamentos y para la biodetección.
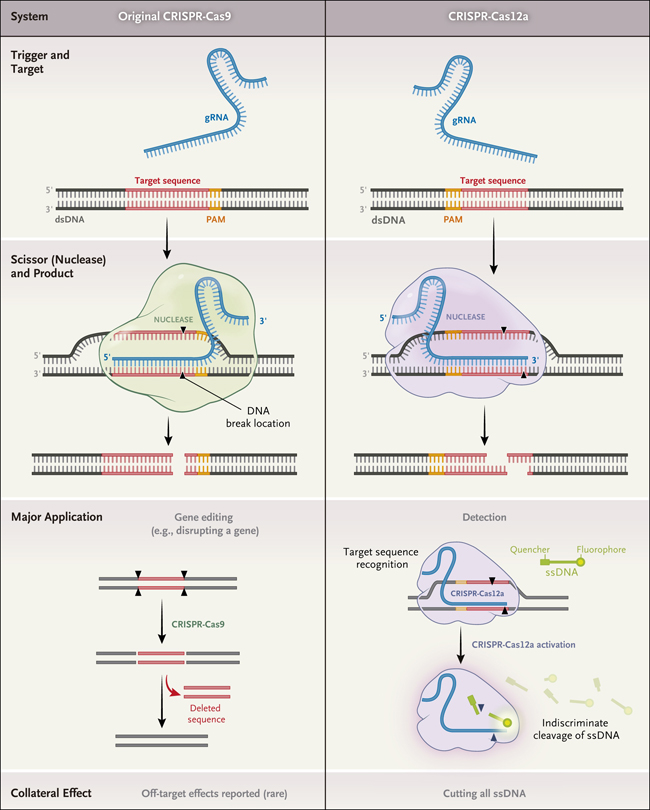
Figura 1. Comparación de dos endonucleasas Cas.
CRISPR denota repeticiones palindrómicas cortas agrupadas y regularmente interespaciadas, dsDNA = ADN de doble cadena, gRNA = ARN guía, PAM = motivo adyacente de protoespaceador y ssDNA = ADN de cadena simple.
En primer lugar, los autores diseñaron el ARN guía para complementar el ADN de doble hebra "desencadenante" (figura 2); por lo tanto, el clivaje por Cas12a solo podría ocurrir en presencia de este ADN desencadenante específico. Luego fabricaron hidrogeles con el complejo ARN-Cas12a guía incrustado en una estructura reticular compuesta de ADN de hebra simple. Cuando los sistemas del gel se expusieron al ADN doble hebra de activación, la nucleasa de Cas12a se activó. Cuanto mayor era el número de ADN de doble cadena desencadenante (o cuanto mayor era la duración de la exposición del gel al desencadenante), mayor era el número de moléculas de Cas12a activadas, y mayor era el daño colateral del ADN de hebra simple. Además, mayor era el grado de digestión del andamiaje del gel y la liberación de cargas encapsuladas, como enzimas, nanopartículas que contienen fármacos y células vivas.
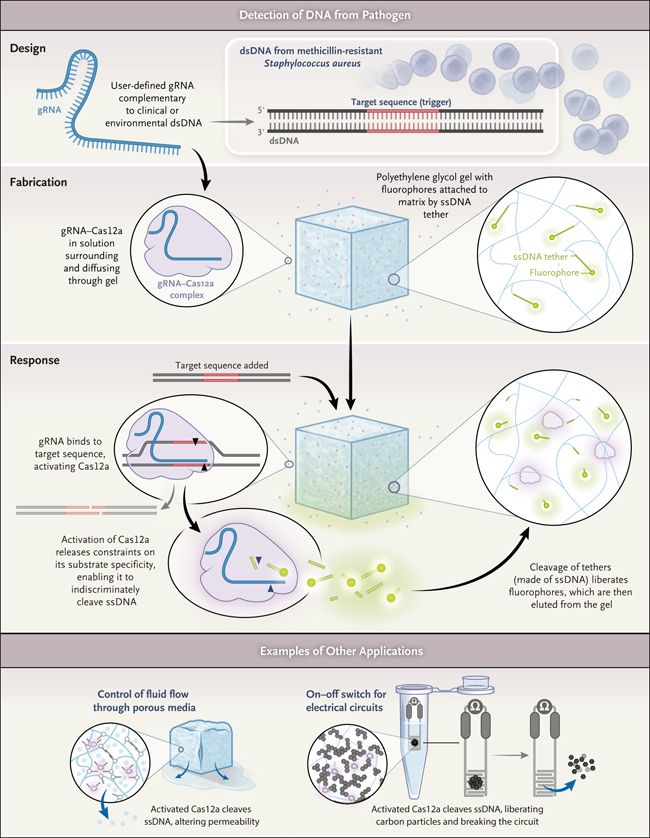
Figura 2. Gel CRISPR como Biosensor.
English y sus colaboradores describieron la fabricación de diferentes tipos de hidrogeles CRISPR que podrían ser potencialmente utilizados como biosensores (por ejemplo, para detectar Staphylococcus aureus resistente a la meticilina o el virus del Ébola) o como sistemas de administración de fármacos y células. En el primer ejemplo que se muestra, la Cas12a activada rompe el ssDNA que está ligado a fluoresceína apagada en un gel de polietilenglicol, lo que resulta en la liberación de la fluorescencia. Los autores también mostraron que la permeabilidad de un gel de poliacrilamida-ADN aumentó (incrementando así la velocidad a la que el fluido fluye a través de él) al exponerse a la Cas12a activada (panel inferior, izquierda) y que un fusible hecha de nanopartículas conductoras de carbono negro reticuladas con ADNss se disparó al exponerse a la Cas12a activada (panel inferior, derecha).
En cuanto a la biosensibilidad, los autores demostraron que podían detectar fragmentos de mecA, un gen que confiere resistencia a la meticilina en el Staphylococcus aureus, uniendo una fluoresceína apagada (el reportero) a un extremo de un ADN monocatenario (figura 2), y el otro extremo del ADN monocatenario a un hidrogel de polietilenglicol (formando una especie de "pendiente" molecular compuesto por una hebra de ADN monocatenario con fluoresceína apagada en el extremo). En presencia del gen mecA de doble hebra (el disparador) y de ARN guía de Cas12a (siendo la secuencia del ARN guía complementaria a parte de mecA), se liberó la carga de fluoresceína. También se han diseñado geles de tal manera que el corte de ADN de hebra simple (desencadenado, por ejemplo, por el ARN genómico sintético del virus del Ébola) resultó en la alteración de la permeabilidad o incluso en la degradación completa del gel. Utilizando estos cambios en las propiedades, mostraron que un gel CRISPR, incrustado en un dispositivo basado en papel microfluídico, podía detectar el ARN sintético del virus del Ébola. Probaron este método pidiendo a cada uno de los tres experimentadores en diferentes lugares geográficos que utilizaran el dispositivo para analizar 12 muestras de ARN sintético del virus del Ébola o blancos como controles. Todas las muestras fueron asignadas correctamente.
Las mayores fortalezas del sistema descrito por English y sus colaboradores son la facilidad con la que se puede adaptar y su capacidad para producir geles programables a partir de materiales tradicionales como la poliacrilamida y el polietilenglicol. Con docenas de proteínas Cas naturales conocidas, medios sencillos para ajustarlas a través de la mutagénesis y muchas -quizás miles- de diferentes enzimas de procesamiento de ADN, uno solo puede imaginar cuántos materiales más podrían diseñarse para entornos clínicos.
Fuente bibliográfica
A CRISPR Path to Cutting-Edge Materials
Ming Chen, M.D., Ph.D., and Dan Luo, Ph.D.
Department of Clinical Laboratory Medicine, Southwest Hospital, Third Military Medical University (Army Medical University), Chongqing, China (M.C.) & Department of Biological and Environmental Engineering, Cornell University, Ithaca, NY (D.L.).
NEJMcibr1911506