Mutaciones que redefinen estrategias terapéuticas en glioma
La enzima IDH modificada es fundamental en la progresión tumoral, especialmente en gliomas. La combinación de inhibidores de mIDH con terapias que activan las células T emerge como un enfoque prometedor para mejorar la eficacia del tratamiento en este y otros tipos de cáncer.
Las variantes monoalélicas somáticas de un solo nucleótido en los genes que codifican la enzima isocitrato deshidrogenasa (IDH) 1 y 2 se encuentran en un gran subconjunto de gliomas de infiltración difusa, así como en ciertos tipos de leucemia aguda y otros tumores sólidos. La variante más prevalente en los gliomas causa un cambio de aminoácido en la posición 132 de la proteína IDH1 (IDH1R132H), lo que resulta en una nueva actividad enzimática oncogénica. La IDH mutante (mIDH) convierte el α-cetoglutarato en el enantiómero R del 2-hidroxiglutarato (R-2-HG), el cual se acumula en el tejido tumoral hasta alcanzar niveles milimolares elevados. Como oncometabolito, el R-2-HG induce la transformación maligna de las células progenitoras gliales, alterando la estructura de la cromatina mediante una amplia hipermetilación del ADN y de las histonas, así como modificando el metabolismo celular.
Poco después del descubrimiento de las mutaciones de la IDH, se iniciaron varios programas para desarrollar fármacos que inhibieran su actividad enzimática neomórfica, bloqueando así la producción del oncometabolito R-2-HG. Estos esfuerzos llevaron a la aprobación del ivosidenib por la FDA para el tratamiento de la leucemia mieloide aguda, el colangiocarcinoma metastásico y el síndrome mielodisplásico. Recientemente, la FDA también aprobó el vorasidenib, un inhibidor de la mIDH que penetra en el cerebro, tras un ensayo clínico de fase 3 que demostró su eficacia en pacientes con gliomas de bajo grado residuales o recurrentes. Ambos inhibidores son capaces de revertir la desregulación celular asociada al R-2-HG e inducir la rediferenciación de células tumorales en modelos preclínicos y en células de pacientes.
Los modelos preclínicos y los estudios de fase 0 han demostrado que bloquear la producción de R-2-HG aumenta la infiltración y actividad de las células T en los tumores. Esta relación apoya hallazgos que indican que la IDH mutante, además de su papel oncogénico, suprime las respuestas inmunitarias antitumorales. Además, se sugiere que la R-2-HG inhibe la expresión de quimioquinas y citoquinas en las células de glioma, lo que dificulta el reclutamiento de células inmunitarias. Estos efectos contribuyen a un microambiente inmunitario con escasas células inmunitarias activadas en gliomas con IDH mutante, en comparación con los tumores que presentan la IDH de tipo salvaje.
Un estudio reciente de Wu y colaboradores del Hospital General de Massachusetts y la Universidad de Harvard, en EE. UU., desarrolló un modelo de ratón genéticamente modificado para cáncer de hígado con mIDH. Se demostró que el ivosidenib provoca una rápida desmetilación del ADN, detiene la proliferación de las células tumorales y promueve la infiltración de células T CD8+. Además, los análisis transcripcionales longitudinales mostraron una activación rápida y sostenida de las vías de respuesta al interferón y de características inflamatorias y virales asociadas, lo que sugiere un mecanismo intrínseco de estimulación inmunitaria. Esta respuesta viral se relacionó directamente con la inhibición de mIDH, no como un efecto de mayor detección de interferón.
¿Cómo induce el ivosidenib las vías de respuesta viral?
La respuesta celular a los virus se inicia a través de mecanismos de detección que activan la transcripción de interferones, los cuales tienen funciones antivirales, antiproliferativas e inmunomoduladoras. Un componente clave del sistema inmunitario es la capacidad de detectar ADN citosólico foráneo. La GMP-AMP sintasa cíclica (cGAS) es el sensor principal que detecta ADN bicatenario en el citosol, activando STING para promover la producción de interferones y otros genes inmunomoduladores. cGAS detecta tanto el ADN invasivo viral como el endógeno similar al viral (mimetismo viral). Este estudio relaciona la activación de la respuesta al interferón por inhibidores de mIDH con el mimetismo viral. Se demostró que en tumores hepáticos y cerebrales con mIDH1, la cGAS está silenciada por hipermetilación. La inhibición de la IDH mutante promueve la desmetilación del ADN, reactivando el promotor de cGAS y elementos transponibles. Este proceso se ve potenciado por el interferón-γ de las células T, creando un ciclo de retroalimentación que fortalece la inmunidad antitumoral (figura 1).
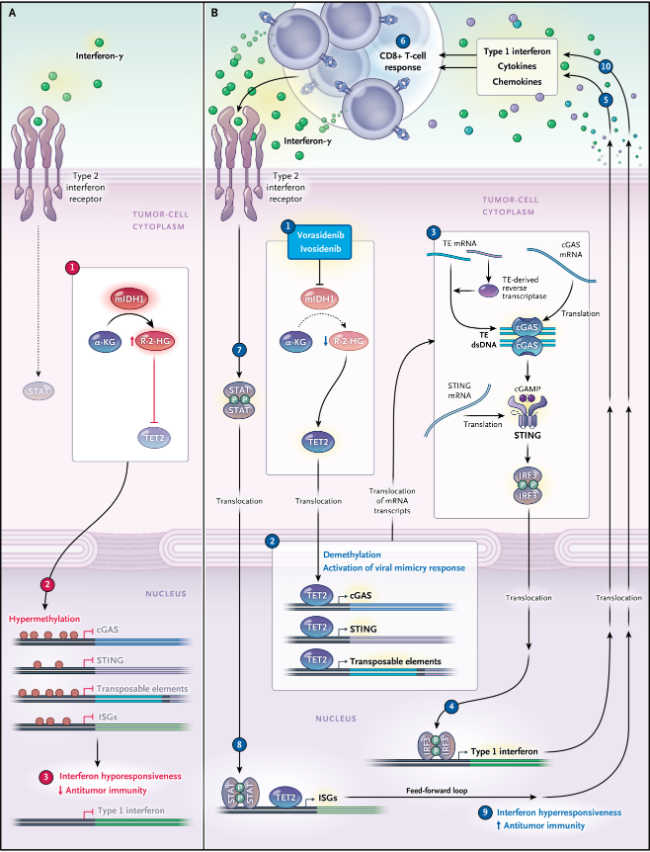
Figura 1: inmunidad, actividad transcripcional y crecimiento de tumores con IDH mutante.
En resumen, la investigación de Wu y sus colaboradores resalta cómo los defectos epigenéticos intrínsecos de las células tumorales impulsan la evasión del sistema inmunitario, favoreciendo así la progresión de tumores con mutaciones en IDH1. Es plausible especular que los efectos inmunosupresores de la mIDH conducen a la evasión inmunitaria, lo que permite la gliomagénesis, a pesar de que IDH1R132H actúa como un neoepítopo inmunogénico.
¿Cuáles son las implicaciones clínicas del estudio?
Estos hallazgos refuerzan la justificación para combinar inhibidores de mIDH con terapias que activan las células T, como vacunas específicas para mIDH1 o inhibidores de puntos de control inmunitario, como sugieren datos preclínicos. Además, los efectos inmunoestimulantes podrían intensificarse mediante terapias que amplifiquen el mimetismo viral. Por último, la implicación de la vía cGAS en la regulación de la inmunidad tumoral podría proporcionar un biomarcador adicional para evaluar la respuesta a los inhibidores de mIDH en pacientes con glioma y otros tipos de cáncer.
Fuente bibliográfica
Heating Up IDH-Mutant Gliomas
Michael Platten, M.D. and Lukas Bunse, M.D., Ph.D.
Department of Neurology, Medical Faculty Mannheim, Heidelberg University, and the German Cancer Research Center
N Engl J Med 2024; 391:2170-2172