Metilación contra el neuroblastoma
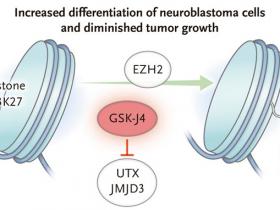
El neuroblastoma de alto riesgo a menudo se distingue por la amplificación del gen MYCN y la pérdida del potencial de diferenciación celular. Un reciente estudio realizó un cribado farmacológico de alto rendimiento de las terapias enfocadas en parámetros epigenéticos a través de un panel de células tumorales. Se descubrió una hipersensibilidad de las células del neuroblastoma a GSK-J4, un inhibidor de enzimas histona demetilasasa, lo que favorece una mayor metilación en una histona específica (H3K27), resultando en un aumento de la diferenciación y en la disminución del crecimiento tumoral.
Inhibidor de histona demetilasa
El neuroblastoma es un cáncer infantil del sistema nervioso simpático, con propensión a la metástasis generalizada y a un comportamiento clínico agresivo. Para los pacientes con la llamada enfermedad de alto riesgo (típicamente pacientes de 18 meses de edad o mayores que presentan enfermedad metastásica), la terapia estándar es intensiva, y la patología reaparecerá en aproximadamente el 50% de los niños a pesar del tratamiento.
A nivel genómico, el neuroblastoma de alto riesgo se caracteriza principalmente por alteraciones del número de copias, incluidas las aberraciones cromosómicas segmentarias en la mayoría de los pacientes y la amplificación de alto nivel del gen MYCN en aproximadamente un tercio de los individuos. Las mutaciones puntuales recurrentes se observan con menos frecuencia y parecen estar enriquecidas en genes con funciones epigenéticas (por ejemplo, ARID1A, ARID1B y ATRX). Además, los investigadores han informado previamente acerca de la actividad de los modificadores epigenéticos en estudios preclínicos de neuroblastoma.
Lochmann y sus colegas reportan recientemente hallazgos de un estudio que amplía el repertorio de modificadores epigenéticos que muestran actividad en el neuroblastoma (DOI: 10.1126/scitranslmed.aao4680). Para apreciar la importancia de su estudio, es útil tener una comprensión de la organización de la cromatina y cómo los modificadores epigenéticos influyen en ella. La unidad básica de la organización de la cromatina es la histona, un complejo proteico alrededor del cual se envuelve el ADN para formar un nucleosoma. Estas proteínas pueden ser modificadas en residuos de aminoácidos definidos por acetilación o metilación, y estas modificaciones juegan un papel importante en la regulación de la expresión génica.
Lochmann y sus colegas se centraron en un nuevo compuesto, GSK-J4, que inhibe dos histonas demetilasasas (UTX y JMJD3). UTX y JMJD3 son las únicas enzimas conocidas responsables de eliminar los grupos metilo en la histona H3K27; de esta manera, contrarrestan los efectos del complejo represor polycomb 2 (PRC2), que metila H3K27 (figura 1). En primer lugar, los autores demostraron que, de las cerca de 800 líneas celulares que probaron, aquellas de neuroblastoma eran las más propensas a una reducción de la viabilidad celular después de la exposición a GSK-J4. En experimentos posteriores, confirmaron la actividad de la monoterapia con GSK-J4 en el neuroblastoma en estudios in vitro e in vivo de bajo rendimiento en animales. Delinearon los efectos de GSK-J4 sobre las células del neuroblastoma, incluyendo cambios en la expresión del ARN y aumentos en la metilación de H3K27. Finalmente, identificaron al ácido retinoico (un agente que diferencia células) y al venetoclax (que inhibe la molécula antiapoptótica BCL2) como dos fármacos que mejoran la actividad de GSK-J4.
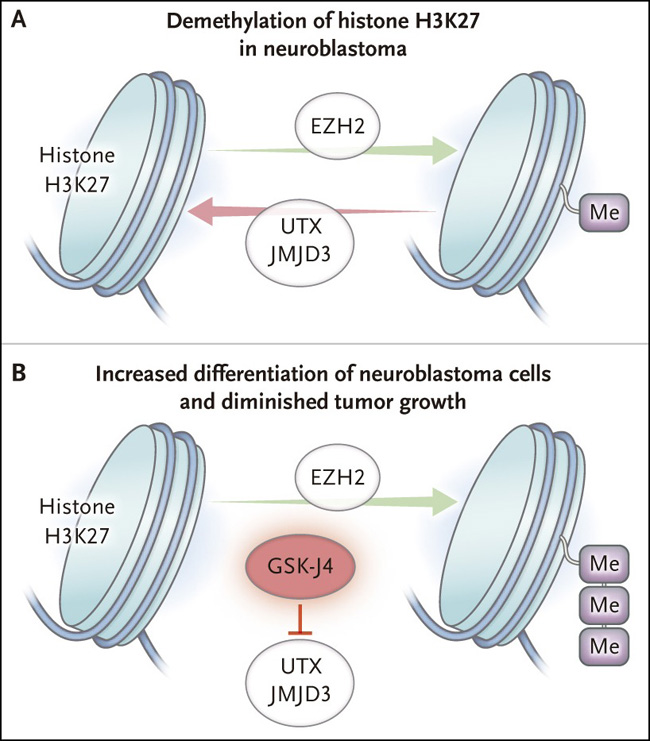
Figura 1. Expresión génica, metilación de histonas y crecimiento de tumores.
El estado de metilación de la histona H3K27 está regulado por la adición de grupos metilo (Me) por la enzima EZH2 y la desmetilación por las histona demetilasasas UTX y JMJD3 (panel A). Lochmann y colegas reportaron recientemente que un medicamento experimental llamado GSK-J4 inhibe la histona demetilasa, inclinando la balanza a favor de una mayor metilación en la histona H3K27 (panel B). En los modelos de ratón de neuroblastoma, este aumento en la metilación resultó en un aumento de la diferenciación y una disminución en el crecimiento del tumor.
¿Cuáles son las implicancias clínicas y translacionales de este estudio preclínico? GSK-J4 aún no está en desarrollo clínico. De hecho, no se tiene conocimiento de ningún otro inhibidor de la histona demetilasa duales UTX, JMJD3 o UTX-JMJD3 que haya sido probado en un ensayo de fase 1. Estudios previos realizados por otros grupos establecieron el papel de GSK-J4 en otro cáncer neural pediátrico devastador, el glioma pontino intrínseco difuso (DIPG, por sus siglas en inglés). El estudio de Lochmann y sus colegas, junto con los hallazgos encontrados en el DIPG, aboga fuertemente por el desarrollo clínico de esta clase de compuestos para el tratamiento de los cánceres infantiles, asumiendo que estudios adicionales aseguren un perfil aceptable de efectos secundarios de estos agentes cuando se administran en dosis efectivas.
Los datos reportados por Lochmann y sus colegas también informan el diseño de ensayos tempranos de inhibidores duales UTX-JMJD3 en el neuroblastoma. GSK-J4 redujo la expresión de MYCN a nivel de transcrito, pero el agente mostró actividad tanto en líneas celulares amplificadas con MYCN como en líneas celulares con MYCN no amplificado. Se necesita investigación adicional para determinar si otros subgrupos (por ejemplo, pacientes con tumores con mutaciones ATRX, ARID1A o ARID1B o pacientes con aumento de la expresión de la proteína MYC) deben ser tratados preferentemente con esta estrategia o si este enfoque puede ser aplicable a todos los subtipos de neuroblastoma. Los hallazgos sugieren ensayos farmacodinámicos que podrían ser incorporados en ensayos tempranos, incluyendo la evaluación de cambios amplios en la expresión del ARN y aumentos en la metilación de H3K27 en tejidos sustitutos. Aunque la eficacia de la inhibición de la histona demetilasa dual está respaldada por los datos, se necesita investigación adicional para entender cómo estos compuestos y combinaciones interactuarían con la quimioterapia citotóxica convencional, una piedra angular actual del tratamiento. Las combinaciones con ácido 13-cis-retinoico y con venetoclax serán informadas por estudios previos que evaluaron el ácido 13-cis-retinoico en combinación con el modificador epigenético vorinostat (ClinicalTrials.gov, NCT00217412 y NCT01208454) y por un ensayo pediátrico en curso de fase 1 sobre venetoclax (NCT03236857).
Desde una perspectiva translacional, este estudio es un recordatorio de que el neuroblastoma es en gran medida una enfermedad de desarrollo aberrante de la cresta neural. Los hallazgos actuales deben motivar estudios adicionales de cambios en la metilación de H3K27 en subtipos clínicos específicos de esta patología y los tumores de ganglioneuroblastoma (que muestran evidencia de diferenciación neural). La edad en el momento del diagnóstico es un indicador pronóstico crítico en el neuroblastoma, por lo que es importante abordar si la metilación en H3K27 está asociada con subgrupos definidos según la edad.
Fuente bibliográfica
Neuroblastoma and Histone Demethylation
Steven G. DuBois, M.D., and Julie R. Park, M.D.
Dana–Farber/Boston Children’s Cancer and Blood Disorders Center and Harvard Medical School, Boston.
DOI: 10.1056/NEJMcibr1806782