Obesidad y el reloj biológico
La obesidad ha alcanzado proporciones de crisis en las sociedades industrializadas. Existen muchos factores que convergen para producir un aumento del índice de masa corporal. Entre ellos se encuentra la duración del sueño. Se sabe que el reloj circadiano controla el dormir a través del proceso de arrastre. Por su parte, el cronotipo describe las diferencias individuales en el ritmo del sueño, que está determinado por los antecedentes genéticos, edad, género y medio ambiente (por ejemplo, exposición a la luz). La descompensación horaria de carácter social cuantifica la diferencia que surge con frecuencia entre los relojes circadianos y sociales, que se traduce en la pérdida crónica de sueño.
El reloj circadiano también regula la homeostasis de la energía, y su interrupción, como ocurre con la descompensación horaria puede contribuir a patologías relacionadas con el peso. En este caso, se ha demostrando que, más allá de la duración del sueño, el desequilibrio se asocia con el aumento del peso corporal. Los resultados demuestran que vivir "contra el reloj" puede ser un factor contribuyente a la epidemia de la obesidad. Esto es de importancia clave en los debates pendientes sobre la aplicación del horario de verano y en los tiempos de trabajo o de escuela, lo que aporta una considerable cantidad de desfase horaria acumulada por un individuo.
Obesidad y control farmacológico del reloj corporal
Nuestros procesos fisiológicos y de comportamiento se organizan en un ciclo de aproximadamente 24 horas. Los ritmos circadianos se producen en casi todos los organismos y es de suponer que reflejan una ventaja evolutiva. Por ejemplo, los seres humanos están preparados fisiológicamente para la actividad y la ingesta de alimentos durante el día, y ayunar y recuperarse en la noche.
Son endógenos, persistiendo en la ausencia de cambios en el medio ambiente o en los comportamientos del día y la noche. Su fuerza es el mejor ejemplo que nuestros comportamientos se producen en el "peor" momento de acuerdo con nuestro reloj interno del cuerpo. Por ejemplo, las personas con descompensación horaria comen y tratan de dormir en fases circadianas inusuales, y esto a menudo causa náuseas y fatiga. Los trabajadores nocturnos pueden tener continuos síntomas de descompensación horaria, lo que conduce al insomnio, enfermedades cardiovasculares, hipertensión, obesidad y diabetes. De interés, por lo tanto, es un reciente estudio realizado por Laura A. Solt y colaboradores (Nature 2012; 485:62-8) sobre compuestos sintéticos que alteran los ritmos circadianos.
En los mamíferos, existe un marcapasos circadiano central en el núcleo supraquiasmático del hipotálamo que orquesta los ritmos circadianos en muchos procesos fisiológicos y de comportamiento. Éste se inicia y se mantiene dentro de las neuronas del núcleo supraquiasmático por un reloj molecular que implica una secuencia de eventos que forman un bucle de realimentación de transcripción-traducción (en el que la traducción de una proteína inhibe, a través de vías directas o indirectas, la transcripción del gen que codifica dicha proteína). Esta secuencia de eventos que dura aproximadamente 24 horas, incorpora oscilaciones en la expresión de proteínas claves, tales como CLOCK, BMAL1, PER, CRY y NPAS2. Dos receptores nucleares, REV-ERB-α y REV-ERB-β, ayudan a regular las oscilaciones de BMAL1 y CLOCK y, por tanto modulan la ritmicidad circadiana. Las células y los tejidos periféricos poseen el mismo reloj molecular, y los ritmos circadianos periféricos suelen estar sincronizados por el marcapasos central a través de las influencias indirectas neuronales, humorales y de temperatura. Lo que no se ha dilucidado, es cómo se produce la coordinación a través del cuerpo.
El reloj del núcleo supraquiasmático normalmente se ajusta a los cambios estacionales durante el día. Este ajuste es causado por los efectos de los estímulos de temporización (llamado zeitgebers o sincronizadores) como la luz. Sin embargo, la fase del marcapasos central en el núcleo supraquiasmático puede tomar varios días para adaptarse, cuando estos zeitgebers se producen fuera de la sincronización, como por ejemplo después de los rápidos cambios de luz-oscuridad que se producen en los viajes de avión a través de zonas horarias o en el trabajo nocturno. Además, puede ocurrir la asincronía interna entre la fase circadiana del núcleo supraquiasmático y la fase de los órganos periféricos debido a las diferencias en la velocidad de reseteo de los relojes centrales y periféricos después de un cambio de comportamiento o zeitgeber.
Los ritmos circadianos del metabolismo son algunas de las armonías más importantes de los mamíferos. El grupo de L. Solt basó su estudio en observaciones anteriores en que la unión de REV-ERB por ligandos alteraba la expresión de genes que regulan el metabolismo de los lípidos y la glucosa, y que ratones knock-out para REV-ERB eran hiperlipidémicos. Por lo tanto, desarrollaron los compuestos SR9009 y SR9011 (agonistas sintéticos de REV-ERB-α y REV-ERB-beta) para determinar si éstos podrían provocar efectos metabólicos beneficiosos en ratones obesos. Los resultados fueron similares para SR9009 y SR9011. En un amplio conjunto de experimentos, ellos encontraron que estos agonistas afectaban el reloj molecular (al inhibir la expresión de BMAL1) y reducían la amplitud de las oscilaciones del ritmo circadiano en explantes in vitro de núcleo supraquiasmático y en fibroblastos. La inyección intraperitoneal de cualquiera de estos agonistas en ratones mantenidos en oscuridad constante generaba una supresión sustancial de la actividad locomotora durante la siguiente noche biológica, cuando los ratones eran normalmente activos (ambos agonistas podían ser detectados en la sangre y en el cerebro después de la inyección). Después de tales inyecciones, los investigadores también encontraron cambios sustanciales en las amplitudes y las fases de los ritmos circadianos de los diversos componentes del circuito de retroalimentación de transcripción-traducción en el hipotálamo.
Era algo impredecible saber cómo estos cambios tan complejos en el reloj molecular se traducirían en alteraciones del comportamiento o la función. Los autores observaron que los efectos de SR9009 y SR9011 sobre la actividad locomotora y la función molecular del reloj en el hipotálamo se atenuaban mucho cuando los ratones eran mantenidos en un ciclo normal de luz-oscuridad, hallazgo que sugería que la entrada de luz se relacionaba con los efectos de la droga.
Entonces, se administraron los agonistas a ratones de peso normal durante 7 a 10 días, lo que resultó en la pérdida de peso (más allá de la observada con la inyecciones control) debido principalmente a la pérdida de masa grasa. Esta caída de peso era causada probablemente por el aumento del consumo de oxígeno; los ratones no mostraron ni aumento de actividad (que disminuyó en un 15%) ni disminución en la ingesta de alimentos (que aumentó un 10% en la noche).
A continuación, separadamente se analizaron la expresión de los genes del reloj molecular y metabólico en músculo, hígado y tejido adiposo blanco después de las inyecciones de REV-ERB-α y REV-ERB-β. Se observaron diferencias en el efecto de estos agonistas en los relojes moleculares del núcleo supraquiasmático y periferia, un hallazgo que sugería una asincronía interna. También se detectó disminución de los niveles de expresión de los genes lipogénicos en el hígado y elevadas concentraciones de enzimas responsables de la oxidación de la glucosa y de ácidos grasos, y el transporte de ácidos grasos en el tejido muscular. En el tejido adiposo blanco, la expresión de los genes implicados en el almacenamiento lipídico era relativamente débil. Estos resultados son consistentes con una supresión de la lipogénesis y la síntesis de colesterol y de ácidos biliares en el hígado, el aumento de los lípidos y la oxidación de la glucosa en el músculo esquelético, y la disminución de la síntesis de triglicéridos y de almacenamiento en el tejido adiposo blanco.
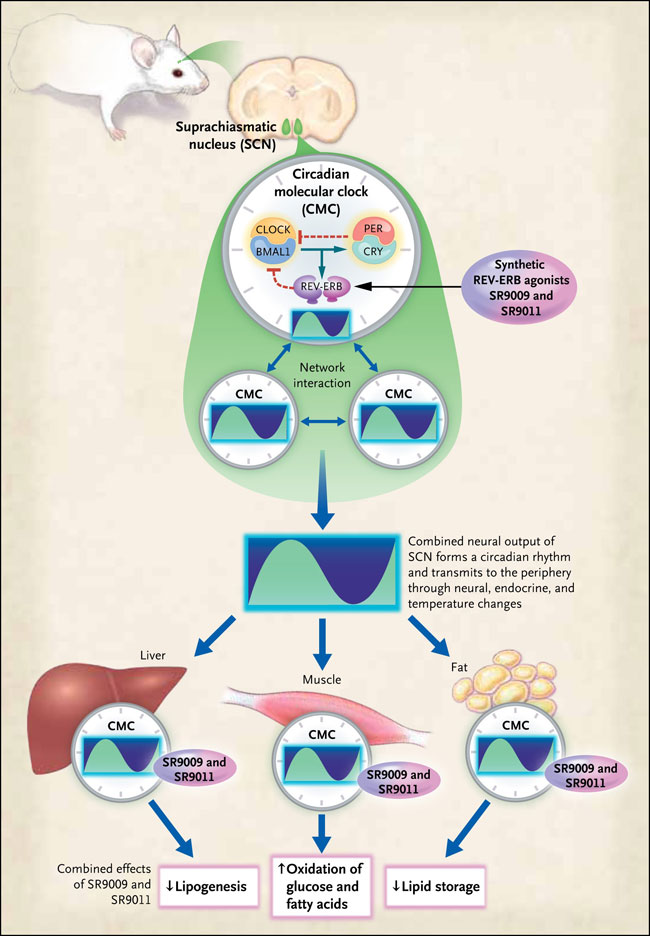
El marcapasos circadiano central se aloja en el núcleo supraquiasmático (SCN) del hipotálamo. El reloj circadiano molecular (CMC) existe en todas las células en el cuerpo y se compone de una extremidad positiva (gobernada por el heterodímero CLOCK-BMAL1) y una extremidad negativa (gobernada por el heterodímero PER-CRY). El sistema está modulado por el receptor nuclear REV-ERB. Las células en el SCN forman una red de interacciones, alterando la actividad de los canales iónicos y, en última instancia, la producción neuronal con ritmo circadiano. Esta salida neuronal circadiana actúa entonces directa o indirectamente (por ejemplo, a través de señales endocrinas intermediarias) para sincronizar las actividades de los órganos periféricos. Sin embargo, las células periféricas también contienen el CMC. Se ha descubierto que los agonistas sintéticos REV-ERB (SR9009 y SR9011) pueden afectar la función de reloj en el SCN y los sitios periféricos, causando la pérdida de peso en ratones obesos.
Basándose en estos impresionantes resultados, los autores concluyeron: la inyección de los agonistas en ratones obesos durante un período de 12 días dio lugar a la reducción de peso (60% más de la observa con las inyecciones control), pérdida de masa grasa y mejora del perfil, incluyendo bajos niveles plasmáticos de triglicéridos, colesterol total, ácidos grasos no esterificados, glucosa e insulina (fig. 1). También hubo una disminución del 80% en la leptina, presumiblemente debido a la pérdida de masa grasa. El grupo de investigadores señaló además que la inyección del agonista sintético REV-ERB reducía los triglicéridos y el colesterol total, incluso en ratones delgados.
Con el uso de REV-ERB, los investigadores han proporcionado evidencia de la modulación farmacológica de los ritmos circadianos - central, periférico y (en varios órganos y tejidos) de manera diferenciada. Los efectos fisiológicos son convincentes, y ofrecen un potencial en humanos, aunque aún quedan muchas interrogantes. En primer lugar, habría que establecer la dinámica de los efectos de la droga en los diversos tejidos. En particular, es importante determinar si los mismos efectos u otros ocurren cuando las inyecciones se producen en momentos diferentes del día y la noche. En segundo lugar, el conocimiento sobre la interacción de estos efectos con los zeitgebers es rudimentario o inexistente. Tercero, los ratones son de actividad nocturna y los humanos diurna, por lo que REV-ERB-α y REV-ERB-β podrían tener efectos opuestos en las dos especies. En cuarto lugar, ¿cuáles serían los síntomas y resultados ocasionados por estos compuestos en seres humanos? Cabe considerar que los ratones "tomaron una noche libre" en su rutina después de la inyección de REV-ERB-α y REV-ERB-β, tal vez debido a los síntomas debilitantes o efectos secundarios. Finalmente, pareciera que la fisiológica y cambios de comportamiento inducidos por los agonistas sintéticos se producen por las alteraciones de ritmo en el reloj molecular central, pero poco se sabe acerca de los mecanismos de transducción de señales desde el reloj central a los efectores fisiológicos y de comportamiento. Todo esto, representa un desafío excitante, en la que los investigadores están trabajando día y noche.
Fuente bibliográfica
Obesity and Pharmacologic Control of the Body Clock
Steven A. Shea, Ph.D.
Oregon Health and Science University, Portland.
N Engl J Med 2012; 367:175-178