La trampa extracelular de neutrófilos
El lupus eritematoso sistémico es una enfermedad autoinmune en la cual los pacientes desarrollan anticuerpos contra el ADN, las histonas, y con frecuencia a las proteínas de los neutrófilos. Estos complejos inmunes, que son patógenos, pueden causar muchas enfermedades, tales como la nefritis lúpica. En los pacientes con lupus, las infecciones generan erupciones y son causa importante de mortalidad. Curiosamente, los neutrófilos también responden a las infecciones mediante el combate de los patógenos extracelularmente, al producir una estructura tipo red en la que quedan atrapados los gérmenes dañinos, así, las denominadas trampas extracelulares de neutrófilos suelen comportarse como antibióticos, y están formadas de ADN, histonas, proteínas y neutrófilos. El oportuno control de estas estructuras extracelulares puede ser crucial en la homeostasis de los tejidos para evitar la presentación de antígenos propios.
Lupus eritematoso sistémico y neutrófilos
La mayoría de los médicos identifica a los linfocitos B y linfocitos T, y tal vez a las células dendríticas, como las unidades implicadas en la patogénesis del lupus eritematoso sistémico (LES). Esta enfermedad autoinmune se caracteriza por la pérdida de tolerancia a los antígenos nucleares, el depósito de complejos inmunes en tejidos, y la afectación multiorgánica. Estudios recientes, como los de Roberto Lande y colaboradores (Sci Transl Med 2011; 3:73ra19) y Gina S. García-Romo y colegas (Sci Transl Med 2011; 3:73ra20), han puesto a los neutrófilos a la vanguardia de la patogénesis de la condición y arrojado señales sobre cómo los eventos bioquímicos y celulares están vinculados.
La activación crónica de las células dendríticas plasmacitoides por complejos inmunes circulantes es un desencadenante clave a comienzos de la autoinmunidad en pacientes con LES. Estos complejos provocan que las células dendríticas plasmacitoides segreguen los interferones tipo I. En el lupus, la prevalencia de la distribución de células dendríticas plasmacitoides se reduce notablemente debido a que éstas migran a los tejidos y permanecen en ellos, sin embargo, residualmente, algunas unidades circulantes pueden producir interferón-α con normalidad y en grandes cantidades, generando un efecto sistémico. Una célula dendrítica plasmocitoide sintetiza unas mil millones de moléculas de interferón-α en un período de 12 horas, 200 a 1.000 veces más que otros tipos celulares. Los estudios genómicos indican que cerca del 95% de los niños y el 70% de los adultos con LES tienen interferón tipo I, en donde el interferón-α es un sello distintivo. El trastorno también se caracteriza por la expresión de genes específicos de neutrófilos, que se correlaciona con la actividad de la enfermedad. Por lo tanto, esta marca genética es la segunda más frecuente en la sangre periférica de células mononucleares en niños con LES. Además, la presencia de proteínas específicas de neutrófilos en orina, un marcador indirecto de la actividad de la enfermedad, puede ser un indicador de su posible papel en la patogenia.
Los estudios realizados por los grupos de R. Lande y G. García-Romo sugieren que una sustancia basada en la cromatina se deposita en la matriz extracelular, sometiendo a los neutrófilos a una única forma de muerte celular - denominada NETosis - representando el vínculo entre la producción de interferón-α y la muerte de neutrófilos. El descubrimiento de esta sustancia, llamada trampa extracelular de neutrófilos (NET), reveló que los neutrófilos pueden inmovilizar y matar a los microbios invasores a través de la formación de la NET. En algunos pacientes, la degradación de la NET se deteriora debido a inhibidores de la DNAsa I o por anticuerpos.
El ensayo de Roberto Lande observó que el péptido antimicrobiano LL-37 - un mediador clave para la activación de células dendríticas plasmacitoides en la psoriasis - se expresa en altos niveles en personas con lupus eritematoso sistémico, sugiriendo que está involucrado en la inmunogenicidad de los ácidos nucleicos en los complejos inmunes. Además, se confirmó que LL-37 y el péptido neutrófilos humanos (PNH) son esenciales para la inmunogenicidad del ADN que contiene los complejos inmunes en el lupus eritematoso sistémico y que el ADN libre entra y activa las células dendríticas plasmacitoides a través del receptor 9 tipo toll formando un complejo con LL-37. Del mismo modo, los anticuerpos en los complejos inmunes interactúan con el receptor Fc gamma II de superficie (FcγRII) en células dendríticas plasmacitoides, provocando la endocitosis del propio ADN.
Los complejos de péptidos antimicrobianos de ADN, LL-37 y el PNH, parecen ser los componentes fundamentales de la NET, ya que activan las células dendríticas plasmacitoides para producir interferón-α (figura 1). Los anticuerpos anti-LL-37 y anti-PNH activan los neutrófilos para liberar la NET, la exposición de los neutrófilos al tratamiento con interferón-α in vitro es seguido por la expresión de los péptidos LL-37 y el PNH. El grupo de R. Lande observó una correlación significativa entre los altos niveles de anticuerpos anti-LL-37, de anticuerpos anti-PNH y la cantidad de anticuerpos anti-ADN, proponiendo que los péptidos antimicrobianos derivados de neutrófilos actúan como autoantígenos de células B en conjunto con el ADN.
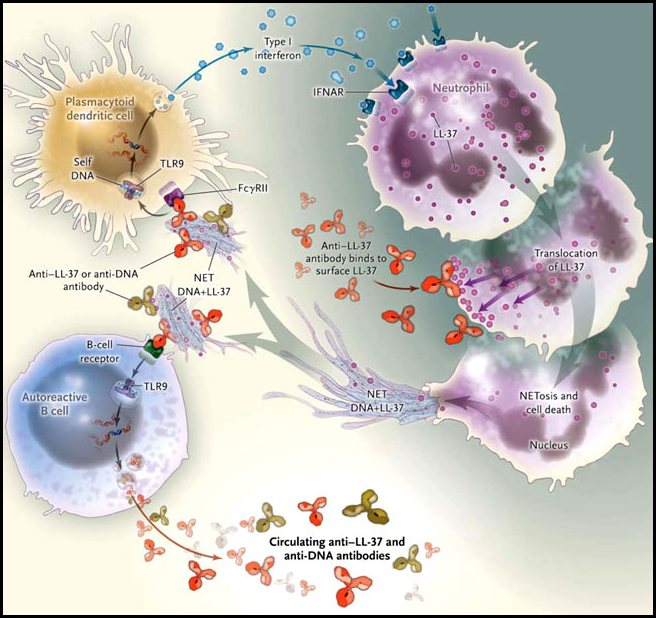
La liberación de la trampa extracelular de neutrófilos (NET) por los neutrófilos y la activación de las células dendríticas plasmacitoides controlan la producción crónica de interferón-α observada en el LES. Los interferones tipo I conducen a los neutrófilos a la NETosis, con desplazamiento de LL-37 a la superficie. La NETosis comienza por la unión superficial de LL-37 a autoanticuerpos anti-LL-37. Las NET liberadas a partir de neutrófilos muertos son absorbidas por las células dendríticas plasmacitoides como una red asociada al complejo inmune LL-37-ADN, junto con anticuerpos anti-LL-37 o anti-DNA. El ADN asociado a NET se involucra con el receptor 9 tipo toll (TLR9) en los endosomas, dando lugar a la liberación de interferón y de neutrófilos adicionales. Por otra parte, los péptidos antimicrobianos derivados de neutrófilos, como LL-37, se utilizan como autoantígenos de las células B en combinación con el ADN. Como resultado, la mayor cantidad de NET también puede incitar a la activación de células B autorreactivas, posiblemente a través de la capacidad de la NET para estimular receptores de las células B y TLR9 en células B, que conduce a la liberación de los anti-LL-37 y anticuerpos anti-DNA. IFNAR denota receptor interferón-α tipo I.
Por otra parte, la investigación de García-Romo también mostró que la NET en el LES contienen LL-37, demostrando que los complejos inmunes albergan autoanticuerpos anti-ribonucleoproteína unidos con FcγRIIA en neutrófilos con muerte por NETosis, generando la producción de especies reactivas del oxígeno. También observaron que, en última instancia, estos hechos llevan a la activación de las células dendríticas plasmacitoides, y por lo tanto, a la secreción de interferón-α.
Estos hallazgos sugieren que, en el LES, los anti-anticuerpos activan los neutrófilos, modificando la NET que a su vez contiene complejos de ADN y péptidos antimicrobianos. Estos complejos activan las células dendríticas plasmacitoides, liberando interferón-α y exacerbando o perpetuación la inflamación y la enfermedad. Las bases moleculares de la formación de la NET no están claras, aunque se sabe que las especies reactivas del oxígeno desencadenan la activación de las enzimas de neutrófilos y su reubicación en el núcleo para iniciar la anulación del ADN, dependiente de formación de la NET. El aumento de la producción de especies reactivas del oxígeno, tales como el anión superóxido y el peróxido de hidrógeno, se asocia con el LES, como se observa en las proteínas modificadas por oxidación, la peroxidación lipídica y la oxidación de las lipoproteínas.
¿Podría la supresión de la NET como resultado de la compactación de especies reactivas del oxígeno detener la autoinmunidad crónica en pacientes con lupus eritematoso sistémico? El yodonio difenil (un potente inhibidor de la NADPH oxidasa que impide la generación de radicales libre de oxígeno derivados en los neutrófilos) afecta profundamente la formación de la NET. El glutatión, un limpiador de peróxido de hidrógeno, inhibe la muerte de neutrófilos; y la catalasa, que reduce el peróxido de hidrógeno en agua, retrasa la apoptosis normal de los neutrófilos.
La interferencia específica en la señalización de los receptores tipo toll también podría convertirse en un atractivo objetivo para el tratamiento del LES, en donde frecuentemente la terapia incluye medicamentos inespecíficos con inmunosupresión tóxica. Por ejemplo, la hidroxicloroquina, que inhibe la señalización a través de los receptores tipo toll 3, 7, 8 y 9, es eficaz en el LES, y la inhibición de los receptores tipo toll 7 y 9 mitiga la manifestación de la enfermedad en ratones.
Queda por demostrar si la NETosis puede servir como un biomarcador o predictor de daño tisular en el LES y si la mayor NETosis, que se produce en algunas vasculitis, es un factor presente en otras enfermedades autoinmunes asociadas a la producción de autoanticuerpos, con la firma del interferón, o daño vascular, como en el síndrome de Sjögren, la artritis reumatoide o las miopatías inflamatorias.
Fuente bibliográfica
Systemic Lupus Erythematosus and the Neutrophil
Xavier Bosch, M.D., Ph.D.
Department of Internal Medicine, Hospital Clinic, University of Barcelona, Institut d'Investigacions Biomèdiques August Pi i Sunyer, Barcelona.
N Engl J Med 2011; 365:758-760