Erk1 y Erk2:
Reguladores de la fertilidad femenina
En el ovario de los mamíferos, las células germinales femeninas (ovocitos) residen en los folículos ováricos y están rodeados de células somáticas derivadas de las células de la granulosa y del cúmulo, teniendo funciones endocrinas y el control de maduración de ovocitos. El éxito reproductivo de las mujeres depende del crecimiento de los folículos ováricos y la diferenciación de las células de la granulosa, así como la maduración de ovocitos y la ovulación. Aunque la hormona luteinizante desempeña un papel fundamental en el inicio de la ovulación y en la diferenciación terminal de las células granulosas hacia células lúteas que componen el cuerpo lúteo y producen progesterona, las principales dianas moleculares en estos procesos siguen siendo aún desconocidas.
Hormona luteinizante y ovulación
La ovulación, que comienza con el aumento de la hormona luteinizante, culmina en la ruptura del folículo ovárico y continúa con la entrega de un óvulo maduro. Este evento, preludio de la fertilización, es foco constante de curiosidad, interés e investigación en el área de la reproducción. Heng-Yu Fan y colaboradores (Science 2009; 324(5929):938-941) descubrieron recientemente en ratones que dos moléculas de señalización - las quinasas 1 y 2 reguladas por señales extracelulares (Erk1 y Erk2) - son fundamentales para la ovulación inducida por la hormona luteinizante.
La respuesta ovulatoria en mamíferos representa una compleja serie de eventos que consta de por lo menos cuatro componentes: reanudación de la meiosis (también conocida como la maduración de ovocitos), expansión y mucificación del cúmulo ooforo, desplazamiento de la producción de estrógeno folicular a la producción de progesterona (luteinización de las células granulosas) y la desintegración de la pared del folículo, que permite la liberación del óvulo (figura 1). Se ha demostrado que Erk1 y Erk2 regulan el efecto de la hormona luteinizante sobre la expansión de cúmulo y la maduración de los ovocitos (demostrado in vitro con el uso de cultivos de cúmulos ovocitos y el aislamiento de folículos ováricos intactos). Por otra parte, un estudio de células de granulosa sugiere que Erk1 y Erk2 controlan la ruptura de la comunicación celular inducida por la hormona luteinizante, requisito previo para la maduración de los ovocitos (figura 1). Sin embargo, a través de su estudio, H. Y. Fan y colegas han encontrado que Erk1 y Erk2 son moléculas esenciales para todo el conjunto de respuestas que resultan en la ovulación.
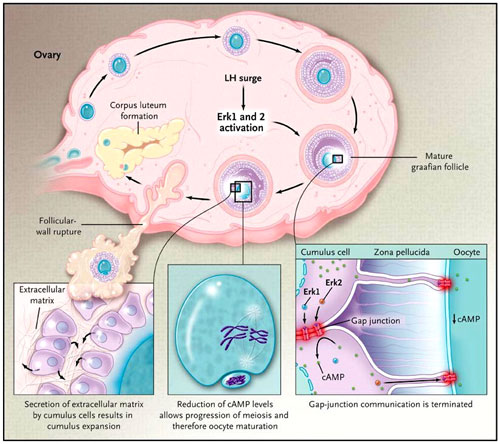
H. Y. Fan y colaboradores encontraron que la hormona luteinizante (HL) induce la ovulación en ratones a través de las quinasas Erk1 y Erk2. Este estudio, junto a otros, sugiere que Erk1 y Erk2, en respuesta a la exposición folicular a HL, fosforila la denominadas proteínas de uniones comunicantes en las células granulosas y en el cúmulo, lo que lleva a una disminución del flujo molecular, como el AMP cíclico (AMPc), tanto en estas células como en células del cúmulo y del óvulo. En el ovocito, el AMPc reprime la reanudación de la meiosis y, por tanto, la maduración. Una reducción del AMPc en el ovocito reanuda la meiosis y, por consiguiente, la maduración de los ovocitos. Por último, la mucificación de las células del ovocito también depende de Erk1 y Erk2. Estas proteínas regulan la rotura de la pared folicular y la formación del cuerpo lúteo.
El estudio representa un modelo de ratón para la infertilidad femenina, ya que éstos no producen Erk1 o Erk2, concretamente, en las células de la granulosa (y también en las células del cúmulo, que derivan de las células granulosas). La inmadurez sexual femenina de estos ratones mutantes no les permite ovular y son totalmente estériles. Sus ovarios contienen folículos preovulatorios pero no cuerpo lúteo y, en consecuencia, las concentraciones de estradiol son elevadas, mientras que los niveles de progesterona se mantienen bajas. También se observó una falta de respuesta a la hormona luteinizante cuando se trataron con hormonas exógenas; sus ovocitos permanecieron meióticamente detenidos, y el cúmulo ooforo no se expandió. Tampoco se produjo ruptura del folículo.
Este estudio señala que Erk1 y Erk2 son reguladores maestros de la fecundidad capaces de moderar el efecto de la hormona luteinizante en todos los componentes de la respuesta ovulatoria: la maduración de los ovocitos, la expansión del cúmulo, la luteinization y la ruptura del folículo. Estos resultados parecen sugerir que cualquier defecto en la vía de transducción de señal de Erk1 o Erk2 inevitablemente resulta en un fracaso global de la fecundidad que no puede ser tratado con hormonas exógenas. Sin embargo, como se demuestra aquí, si la patología molecular se limita a células somáticas del folículo ovárico, el ovocito es plenamente capaz de reanudar la maduración meiótica: cuando los autores aislaron físicamente ovocitos del folículo ovárico, éstos maduraron espontáneamente, deteniéndose en la metafase II.
El grupo de H. Y. Fan intentó diseñar ratones carentes de Erk1 y Erk2 sólo en células somáticas del folículo ovárico, esperándose que los ovocitos expresaran Erk1 y Erk2, lo que llevaría a preguntarse si esta estrategia "rescata" la fertilidad en mujeres infértiles a causa de una aberración en esta vía de señalización. Tal error presumiblemente afectará a todos los tipos de células, incluidas las del óvulo. Sin embargo, se desconoce si la señalización de Erk1 y Erk2 participa en la primera división meiótica, aunque si se sabe que regula la detención de la metafase de la segunda división meiótica.
Por lo tanto se podría prever una estrategia para recuperar la fertilidad - por aspiración del óvulo desde el folículo ovárico - presumiblemente como resultado de la reanudación de la meiosis espontánea. Los ovocitos sometidos a maduración in vitro se identifican por la presencia del primer cuerpo polar. Estos ovocitos pueden ser sometidos a fecundación in vitro, seguido de la transferencia de embriones. La ausencia de un cuerpo lúteo podría necesitar un suplemento de progesterona para mantener el embarazo durante el primer trimestre. Por supuesto, el éxito de esta estrategia depende de muchos factores que aún no se han descrito, tales como si ERK1 y ERK2 en mujeres imitan sus genes ortólogos en ratón y si la inactivación de las vías de ERK1 y ERK2 (por ejemplo, por una mutación) cause infertilidad masculina.
Fuente bibliográfica
Master Regulators of Female Fertility
Nava Dekel, Ph.D.
Department of Biological Regulation, the Weizmann Institute, Rehovot, Israel.
N Engl J Med. 2009 Aug 13; 361(7):718-9