¡Los cardiomiocitos se regeneran!
El daño miocárdico crónico a menudo produce insuficiencia cardíaca debido a la pérdida y falta de regeneración de los cardiomiocitos. Esto ha impulsado esfuerzos para elaborar su sustitución mediante terapias de trasplante celular o por la activación de procesos de regeneración endógena. El desarrollo de estrategias de trasplantes de células está avanzando rápidamente, y algunas metodologías están siendo evaluadas en ensayos clínicos. Estimular los procesos de regeneración endógena es atractivo ya que podrían proporcionar terapias no invasivas y eludir la inmunosupresión necesaria en los aloinjertos. Sin embargo, no está claro si tales técnicas son realistas ya que ha sido difícil determinar si se pueden generar cardiomiocitos después del periodo perinatal en los seres humanos.
Las células musculares del corazón se dividen y expanden de forma activa en el embrión, pero, tras el nacimiento, perderían esta capacidad proliferativa de forma permanente, al menos eso se creía.
Renovación cardiomiocítica
La capacidad del corazón para regenerar la función del miocardio es muy limitada o inexistente. Esta falta de capacidad regenerativa contrasta con la de muchos otros órganos y tejidos. La insuficiencia cardíaca sigue siendo la principal causa de hospitalización en los Estados Unidos, y su prevalencia crece a medida que la población envejece. En la mayoría de los pacientes, el origen subyacente es una pérdida de cardiomiocitos, acompañado por desarreglos funcionales en la contracción y relajación. La visión tradicional ha sostenido que la capacidad de reparación del corazón se ve limitada por la incapacidad de los cardiomiocitos maduros a someterse a la división celular después de las primeras semanas de vida y a un fracaso en la movilización de las células madre cardíacas (si existen). Sin embargo, un reciente estudio realizado por Olaf Bergmann y colegas (Science 2009; 324(5923):98-102) llama la atención al respecto.
Los investigadores realizaron un experimento midiendo la incorporación de carbono-14 en el ADN genómico de los cardiomiocitos para calcular las tasas de recambio en estas células. Los niveles de carbono-14 en la atmósfera aumentaron bruscamente como consecuencia de los ensayos nucleares y posteriormente cayeron fuertemente una vez que el Tratado de Prohibición de Ensayos Nucleares fue firmado en 1963. Como resultado, las células "nacidas" en tiempos de altas concentraciones de carbono-14 pueden ser precisamente fechadas porque las personas que vivieron durante ese período incorporaron carbono-14 en el ADN de los cardiomiocitos generados. Los resultados indicaron que, contrariamente a la enseñanza tradicional, los cardiomiocitos se renuevan durante la vida a una tasa muy baja. A la edad de 25 años, aproximadamente el 1% se reconvierten anualmente, y la tasa de rotación se reduciría al 0,45% a los 75 años. Durante una vida promedio, menos del 50% de los cardiomiocitos se renuevan. Sorprendentemente, a pesar de las importantes demandas metabólicas y orgánicas en el curso de su vida, algunas de estas células sobreviven durante más de medio siglo.
Antes de este estudio, el carbono-14 se utilizó para resolver controversias en relación con el volumen celular en el cerebro y en células grasas. Sin embargo, esta metodología es particularmente difícil cuando se aplica al corazón debido a la heterogeneidad de los cardiomiocitos y de las células no miocíticas del corazón. El grupo de O. Bergmann aisló cardiomiocitos de fibroblastos, de células endoteliales y células de músculo liso vascular. También tuvieron en cuenta que durante la primera década de vida, aproximadamente el 25% de los cardiomiocitos son sometidos a una ronda final de síntesis de ADN sin división celular, resultando en una subpoblación de cardiomiocitos binucleados. Como el corazón sufre hipertrofia (crecimiento celular), los cardiomiocitos pueden someterse a rondas adicionales de síntesis de ADN, sin división, lo que resulta en unidades tetraploides (cuatro juegos de cromosomas) o poliploidía (muchos juegos de cromosomas). Los investigadores, por lo tanto, desarrollaron y aplicaron un método para identificar los núcleos y el ADN de cardiomiocitos, y así medir sólo la incorporación de carbono-14 en los núcleos diploides. Este estudio proporciona la prueba más concluyente hasta la fecha que los cardiomiocitos humanos se renuevan durante la vida posnatal.
Sin embargo, los investigadores no pudieron determinar el origen de la renovación. Por lo menos cuatro fuentes potenciales de células podrían ser responsables de los "nuevos" cardiomiocitos después del nacimiento. Las unidades adultas, consideradas generalmente diferenciadas, pueden volver al ciclo celular y dividirse. Si esta teoría es validada, sugiere que el antiguo programa de regeneración observada en corazones de anfibios y peces pueden utilizarse para beneficio terapéutico en seres humanos. En segundo lugar, las células progenitoras o células madre cardíacas derivadas de médula ósea podrían poseer la capacidad para diferenciarse in vitro en cardiomiocitos y funcionalmente ser probadas después de la lesión cardíaca. Sin embargo, persiste la controversia sobre si células de la médula ósea pueden regenerar la función del miocardio; los ensayos clínicos que han examinado la eficacia de los derivados de médula ósea y células madre circulantes en pacientes con infarto agudo de miocardio han demostrado escasos resultados, sin beneficios a largo plazo. En tercer lugar, investigaciones en roedores sugieren que células derivadas del epicardio embrionario pueden dar lugar a cardiomiocitos. Por último, se han identificado nichos de células progenitoras cardíacas en el corazón humano y en ratones. Estas poblaciones celulares son especialmente heterogéneas, y los nichos siguen estando mal caracterizados. La población de "células progenitoras cardíacas" sigue siendo difícil de producir, al igual que marcadores para la identificación y seguimiento de dichas células. Una pregunta que se mantiene es por qué estas células, si es que existen, no son movilizadas completamente tras el infarto de miocardio o en la insuficiencia cardíaca.
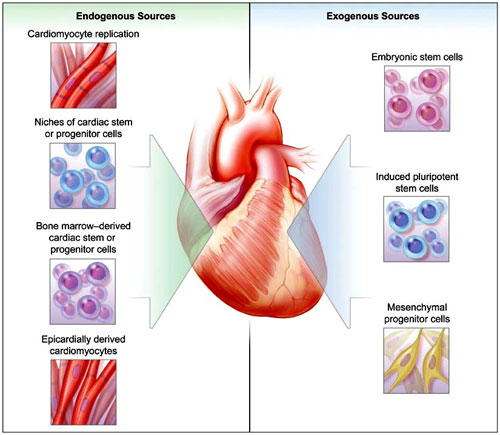
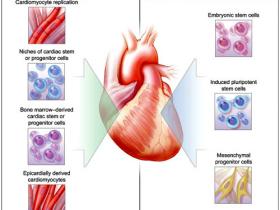
La demostración que algunos cardiomiocitos se regeneran después del nacimiento pone de relieve los desafíos para futuras terapias en la regeneración cardíaca. Fuentes de células autólogas y alogénicas podrían dar lugar a cardiomiocitos.
La demostración que los cardiomiocitos cambian en el corazón adulto pone de manifiesto los desafíos del emergente campo de la medicina regenerativa cardíaca (figura 1). La baja tasa de renovación de los cardiomiocitos observada en el corazón humano revela un formidable obstáculo que deben superar para regenerar la función del miocardio. Por lo tanto, es demasiado pronto para descartar otros enfoques, incluyendo la posible aplicación de células madre embrionarias, células madre pluripotentes inducidas o células progenitoras mesenquimales que puedan ser inducidas para ampliar y diferenciar cardiomiocitos. Sin embargo, sería preferible la activación de una fuente de células autólogas que repueblen funcionalmente el corazón, ya que no plantea la preocupación asociada con el trasplante alogénico de células o la utilización de células madre embrionarias. Es irónico que la devastación ambiental creada por los ensayos de armas nucleares durante la Guerra Fría pueda tener un impacto en el futuro de la medicina regenerativa. En última instancia, el progreso hacia la terapia regenerativa de enfermedades cardíacas debe basarse en un fundamento básico de la biología celular y del desarrollo.
Fuente bibliográfica
Cardiomyocyte Renewal
Michael S. Parmacek, M.D., and Jonathan A. Epstein, M.D.
Cardiovascular Institute, Department of Medicine, University of Pennsylvania, Philadelphia, USA.
N Engl J Med. 2009 Jul 2; 361(1):86-8