Flagelina y factor nuclear kappa B
Cuando el intestino sobreviva a la radioterapia
La toxicidad de altas dosis de radiaciones ionizantes conlleva la inducción de síndromes agudos que afectan al sistema hematopoyético y al tracto gastrointestinal. La extrema sensibilidad de sus células al estrés genotóxico en determina gran medida los efectos secundarios adversos de la terapia de radiación y la quimioterapia contra el cáncer. El desarrollo de radioprotectores y la biodefensa se ha centrado principalmente en los antioxidantes que protejan a los tejidos y a las citoquinas capaces de estimular la regeneración.
En este sentido, se está explorado si la radioprotección puede lograrse mediante la supresión de la apoptosis, el principal mecanismo subyacente de pérdida masiva de células en los tejidos radiosensitivos. En concreto, las actuales investigaciones están tratado de imitar farmacológicamente los mecanismos antiapoptóticos frecuentemente adquiridos por las células tumorales, es decir, la activación constitutiva del factor nuclear kappa B. Esta proteína es un elemento de transcripción que juega un papel fundamental en la respuesta organizacional y celular contra agentes infecciosos a través de la mediación de las reacciones inmunitarias innatas y adaptativas. Recientemente, se ha descubierto en mamíferos el vínculo existente entre el factor nuclear y la respuesta a las radiaciones ionizantes, en donde los ensayos han establecido que la radiosensibilidad del tracto gastrointestinal es mayor en ratones que llevan copias defectuosas de kappa B.
Potencialidad de las bacterias para la protección intestinal
El intestino delgado es un órgano exuberante y dinámico con una variada y compleja gama de funciones vitales. Sus vellosidades y microvellosidades proporcionan una plataforma para la absorción de nutrientes, pero al mismo tiempo, el epitelio y sus células inmunitarias deben mantener alejados a los patógenos que escapan al inhóspito ambiente del estómago. Tal vez como una forma de satisfacer estas responsabilidades, las pequeñas unidades epiteliales intestinales se dividen muy rápidamente, a razón de 13 a 16 células por hora.
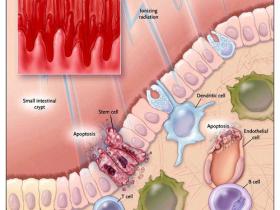
Las radiaciones ionizantes y la quimioterapia juegan un rol de “peaje” en el intestino e inducen la apoptosis de las células madre encargadas de reponer las vellosidades (figura 1). En pacientes que reciben tratamiento para el cáncer, los efectos nocivos de la irradiación en el intestino y la médula ósea pueden obligar a la suspensión de otros tratamientos potencialmente beneficiosos. Recientemente, utilizando un modelo murino, Lyudmila G. Burdelya y colegas (Science. 2008 Apr 11; 320(5873):226-30) pusieron a prueba un nuevo enfoque para proteger al intestino de las lesiones inducidas por irradiación. En concreto, probaron una versión recombinante de la proteína bacteriana flagelina.
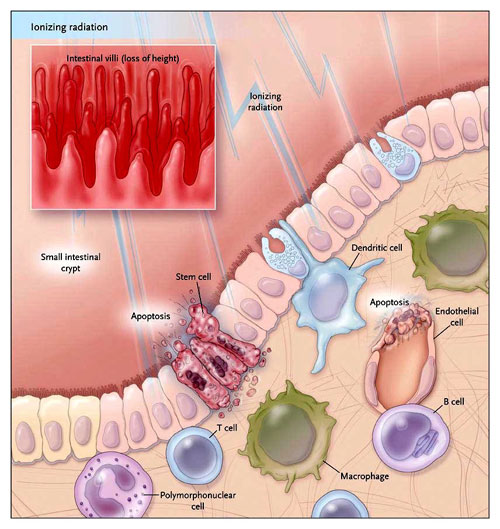
La exposición en el cuerpo de radiaciones ionizantes (como ocurre antes de un trasplante de médula ósea) provoca una masiva apoptosis de las células madre en la base intestinal y de las células endoteliales de los vasos sanguíneos que alimentan el revestimiento del intestino. Este daño se acompaña de una pérdida de altura en las vellosidades intestinales, afectando la capacidad para absorber los nutrientes.
¿Por qué el grupo de Burdelya generó una proteína bacteriana para evitar el daño intestinal? El epitelio del intestino responde a productos bacterianos de una forma muy diferente en comparación a otros órganos. Las bacterias del lumen son necesarias para mantener un intestino sano, de hecho, se ha visto que la proliferación de células intestinales está reducida en ratones libres de gérmenes. Los estudios en estos modelos para la lesión intestinal han demostrado que la respuesta a las bacterias a través de los receptores tipo peaje (o Toll-like receptor, TLRs) es esencial para la correcta reparación del epitelio. Los TLR son miembros de la superfamilia interleucina-1 de receptores transmembrana capaces de reconocer patrones moleculares asociados a patógenos. A su vez, los TLR5 reconocen la flagelina derivada de las bacterias flageladas. La mayoría de los TLR activan el factor nuclear kappa B (NF-kappa B), que tiene efectos pleiotrópicos, incluyendo la inducción de citoquinas y la protección de la apoptosis. Los investigadores pensaron que la estimulación de NF-kappa B con flagelina podría proteger al intestino de las lesiones provocadas por la radiación.
Para probar la hipótesis, primero desarrollaron una proteína recombinante que contenía dos regiones de flagelina necesarias para la activación de TLR5, unidas por un ligando. La inyección de ratones con esta proteína sintética tuvo un efecto dramático sobre la supervivencia después de la irradiación corporal. Incluso la administración del agonista de TLR5 después de la exposición a la radiación protegió a los animales contra la muerte. La irradiación corporal se traduce en masivas apoptosis de las células madre en la base del intestino y de las células endoteliales en la red de vasos sanguíneos que alimentan el revestimiento intestinal. Los resultados de este estudio apoyaron el efecto protector del agonista TLR5 contra la apoptosis del epitelio intestinal y de las células endoteliales. El agonista de TLR5 también fue capaz de proteger a las unidades formadoras de macrófagos-granulocitos en la médula ósea y, por tanto, mitigar los efectos nocivos de la irradiación hematopoyética (figura 2).
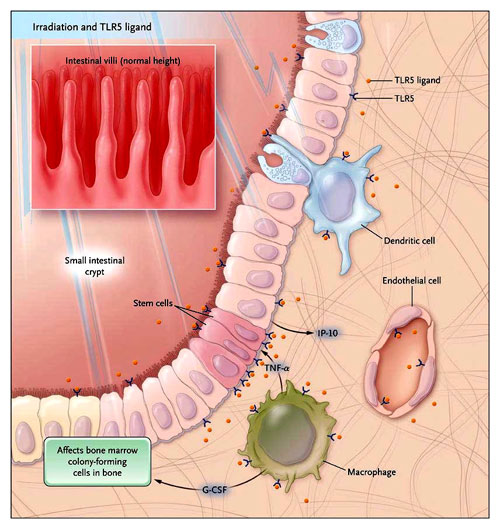
TLR5 se expresa en una variedad de tipos celulares en el intestino; la activación del receptor por un agonista sintético protege contra la apoptosis del epitelio intestinal y de las células endoteliales inducida por irradiación. La unión del agonista conlleva la inducción de citocinas y quimiocinas, como del factor estimulante de colonias de granulocitos (G-CSF), de interleuquina-6 y del factor de necrosis tumoral alfa (TNF-alfa). Este último es conocido por inducir la proliferación de células epiteliales. El agonista también tiene un efecto protector de las células formadoras de colonias en la médula ósea, posiblemente asociado con factores tróficos circulantes. IP-10 representa a la proteína inducible por interferón 10.
En experimentos similares utilizando macacos rhesus, los investigadores observaron que los agonistas de TLR5 aumentaban la supervivencia y tenían efectos protectores sobre la médula ósea, aunque no se proporcionaron datos sobre su efecto en el tracto gastrointestinal de los monos. Sin embargo, hicieron una primera incursión al averiguar cómo TLR5 protegía de los efectos de la irradiación corporal. Encontraron que el agonista inducía una variedad de citocinas y quimiocinas, como el factor estimulante de colonias de granulocitos, interleucina-6 y el factor de necrosis tumoral alfa; este último inducía la proliferación de células intestinales. No está claro, sin embargo, cuando el agonista de TLR5 comienza su “trabajo”. ¿Activa células mononucleares en la sangre periférica, para luego liberar citoquinas y proteger el tubo digestivo y la médula ósea? ¿Actúa principalmente en células inmunitarias en la lámina propia o directamente sobre las células epiteliales intestinales para protegerlas de la apoptosis? ¿Existe un efecto de TLR5 en células mesenquimales de la médula ósea que protejan a las progenitoras hematopoyéticas? Responder estas preguntas puede ser importante a la hora de determinar si se puede administrar por vía oral un agonista TLR5 o tener un efecto tópico sobre las células epiteliales.
Un estudio realizado por Terrence Riehl y colaboradores (Gastroenterology. 2000 Jun; 118(6):1106-16), descubrió los efectos protectores en el intestino de otro ligando TLR, el lipopolisacárido (LPS). LPS es reconocido por TLR4. Los ratones que reciben dosis de LPS antes de la irradiación están protegidos contra la apoptosis de células intestinales por un mecanismo que implica la inducción de la prostaglandina E2. Por desgracia, el lipopolisacárido es demasiado inflamatorio como para utilizarlo sistemáticamente.
Dos posibles preocupaciones surgen en relación al uso de un agonista de TLR para tratar a los pacientes. En primer lugar, existe el riesgo de que su administración imite a la sepsis. A partir de los resultados descritos por el grupo de Burdelya, no es posible determinar si el agonista de TLR5 induce síntomas sistémicos en los monos. Algunos estudios indican que la señalización de TLR puede aumentar la proliferación tumoral. Los investigadores utilizaron el agonista de TLR5 en ratones que tenían tumores y no observaron un mayor crecimiento tumoral o el aumento de radioresistencia. Un potencial problema es que la protección de los precursores de la médula ósea con el agonista de TLR5 también puede impedir la limpieza de células hematopoyéticas malignas en pacientes con cánceres hematológicos.
¿En qué situaciones la terapia con un agonista de TLR5 podría ser útil en los pacientes? Sobre la base del estudio de Burdelya y colaboradores, una real aplicación podría ser su administración antes de la irradiación corporal, que sigue siendo utilizada de forma previa al trasplante de médula ósea. Aunque las dosis de radiación usadas han disminuido en los últimos años, no existe un manejo que evite el daño intestinal inducido por radiación. La irradiación también puede dañar el intestino cuando éste está en el área de un tumor irradiado. Los agonistas de TLR5 también podrían ser beneficiosos en pacientes sometidos a ciertos tratamientos quimioterapéuticos que inducen la apoptosis de células intestinales. Otra posible aplicación, podría ser el uso de un agonista de TLR5 después de la exposición accidental o intencional a las radiaciones de origen nuclear. Si bien se justifican ensayos experimentales adicionales con TLR5 como agente terapéutico, el estudio de Burdelya demuestra que el aprovechamiento de la respuesta inmune innata puede prevenir el daño intestinal.
Fuente bibliográfica
Harnessing the Power of Bacteria to Protect the Gut
Maria T. Abreu, M.D.
N Engl J Med. 2008 Aug 14;359(7):756-9