Neoantígenos: las cartas de presentación del cáncer
La evidencia sugiere que las inmunoterapias clínicamente eficaces contra el cáncer son impulsadas por la reactividad de células T contra los neoantígenos derivados de mutaciones en el ADN. Sin embargo, entre el gran número de neoantígenos predichos, sólo una minoría es reconocida por linfocitos T autólogos de pacientes, por lo tanto, las estrategias para ampliar las respuestas específicas celulares frente a estos péptidos anómalos representan un enfoque muy atractivo. Un reciente estudio evidenció que los repertorios de linfocitos T naïve de donantes sanos proporcionan una fuente de células específicas para neoantigenos, respondiendo a 11 de 57 epítopes de tres pacientes. Muchas de las reactividades de las células T involucraron epítopes que bajo condiciones in vivo fueron inadvertidos por los linfocitos autólogos infiltrantes del tumor de los afectados. Finalmente, estas células redirigidas con receptores de células T identificadas a partir de donantes, reconocieron eficientemente células de melanoma derivadas de personas que albergan mutaciones relevantes, proporcionando una justificación para el uso de enfoques externalizados para potenciar la inmunoterapia contra el cáncer.
Inmunogenicidad tumoral
Aunque los tumores con una alta carga mutacional se han vinculado con un pronóstico desalentador, en la presente era de la inmunoterapia, las mutaciones pueden proporcionar un blanco para el tratamiento citotóxico específico del cáncer. La secuenciación de nueva generación de cientos tipos de tumores ha revelado que ocurren muchas más mutaciones somáticas ocurren en el ADN de las células cancerosas de las que se conocían previamente. Muchas de estas alteraciones ocurren en la región codificante de genes y por lo tanto se transcriben en ARN, que luego es traducido a proteínas. Posteriormente, fragmentos de proteínas pueden aparecer como péptidos alterados, los que son exhibidos por las moléculas HLA en la superficie de células tumorales, donde pueden ser reconocidos como péptidos "foráneos" (llamados neoantígenos) por linfocitos T, de la misma manera que estas últimas perciben péptidos bacterianos.
La eficacia de las inmunoterapias, como los inhibidores de puntos de control inmunológicos (immune checkpoint inhibitors), diseñados para potenciar el propio sistema inmunológico del paciente, se correlaciona con la carga mutacional. Los repertorios de células T que se dirigen a neoantígenos han sido identificados en pacientes y coevolucionado con cambios en el espectro de los neoantígenos en el tiempo. En pacientes tratados exitosamente con inmunoterapia celular adoptiva, las células T que respondían a los neoantígenos desaparecieron concomitantemente con la pérdida de antígeno, mientras que las mutaciones de aparición reciente fueron paralelas por la nueva reactividad de linfocitos T. Estos descubrimientos allanan el camino para nuevas inmunoterapias específicas.
Los neoantígenos candidatos específicos del paciente pueden ser predichos computacionalmente sobre la base de las mutaciones encontradas en el respectivo tumor. Sin embargo, solo un número muy pequeño de neoantígenos candidatos parecen evocar una respuesta inmune en los individuos. De hecho, de los cientos de mutaciones Identificadas en, por ejemplo, el melanoma, que podría proporcionar una gran cantidad de objetivos de células T, se han encontrado sólo unos pocos (entre dos y cinco). Se ha observado un escenario similar con respecto a las células T reactivas al neoantígeno en sangre periférica. Estos están representados casi exclusivamente por linfocitos T que contienen el receptor de muerte celular programada 1 (PD-1), el que al activarse reprime las funciones citotóxicas de las células T. Los receptores de células T (TCR) expresados por este tipo celular han mostrado la capacidad de reconocimiento de tumores autólogos, pero se ha evidenciado que son reactivos solo a una muy pequeña fracción de los neoantígenos candidatos predichos (aproximadamente el 1%). Sin duda la mejora de las respuestas terapéuticas celulares frente a los neoantígenos es una meta muy relevante para la investigación clínica debido a que podría potenciar a los fármacos inhibidores de puntos de control como el nivolumab, que bloquea al receptor PD-1.
Un enfoque creativo e inesperado para abordar estos desafíos fue descrito recientemente por Strønen y sus colegas (Science. 2016 Jun 10;352(6291):1337-41) quienes probaron si las células T de donantes sanos podían reconocer neoantígenos tumorales ser activadas por ellos. Entre las cientos de mutaciones que fueron identificadas por secuenciación del ADN y ARN de tumores de tres pacientes con melanoma, los autores seleccionaron 57 en base a su afinidad con la que los péptidos mutantes se unen al complejo mayor de histocompatibilidad alelo HLA - A * 02: 01. Entonces, los autores sintetizaron fragmentos de ARN mensajero correspondientes a neoantígenos putativos y se introdujeron en células dendríticas derivadas de monocitos (las células presentadoras "profesionales" de antígenos del sistema inmunitario) de un donante sano HLAA *02: 01 positivo.
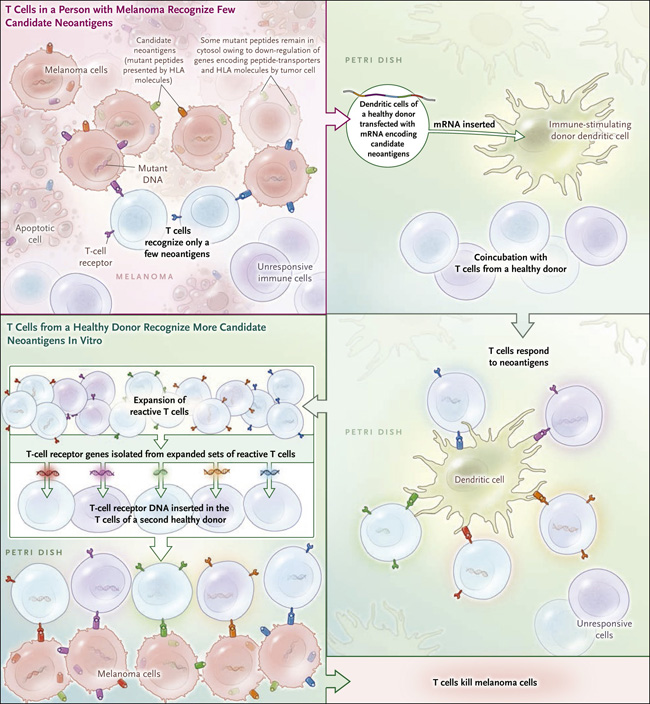
Figura 1: Externalización de la inmunidad contra el cáncer.
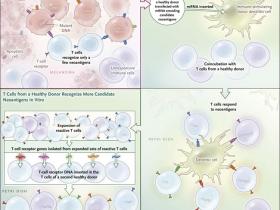
Las células cancerosas albergan muchas mutaciones que producen proteínas alteradas potencialmente inmunogénicas que, sin embargo, no son reconocidas por el sistema inmunitario del paciente. Erlend Strønen y sus colegas mostraron recientemente un medio para identificar respuestas de células T derivadas de donantes a tales mutaciones. Utilizando algoritmos de predicción computarizados, primero seleccionaron neoantígenos candidatos entre los péptidos codificados por genes anómalos a partir de tumores de tres pacientes con melanoma que en teoría parecía probable que sostenían una respuesta inmune. Estos péptidos mutantes se sintetizaron y se expresaron en células presentadoras de antígeno (dendríticas) obtenidas de un donante sano y se incubaron conjuntamente con células T de la misma persona. Los linfocitos T reactivos a los neoantígenos, activados por algunas de estas células dendríticas transducidas, se multiplicaron y los genes del receptor de células T fueron aislados. Los linfocitos T de un segundo donante sano, cuyas células fueron manipuladas genéticamente para expresar receptores reactivos a los neoantígenos, fueron capaces de destruir células tumorales derivadas de los melanomas originales. ARNm denota ARN mensajero.
Los autores probaron in vitro la capacidad de estos antígenos transfectados para inducir la proliferación de células T citotóxicas ingenuas (naive) de los mismos donante de quienes se obtuvieron las células dendríticas. Los tres pacientes presentaron respuestas de células T frente a sólo 2 de los neoepítopes, mientras que las células T del donante sano fueron activadas por 11 de los neoepítopes. Clones de las células T que respondían a los neoepítopes respondieron a bajas concentraciones del mutante y no la versión de tipo silvestre del antígeno. Las secuencias de TCR fueron identificadas y transferidas genéticamente a las células T de un segundo donante sano. El potencial terapéutico de tales células T modificadas con TCR se demostraron por su capacidad para eliminar células de melanoma del paciente HLAA *02: 01 positivo, del que se derivaron originalmente las mutaciones (figura 1).
Estos experimentos muestran que las células T de la sangre de un donante sano representa una valiosa plataforma para probar la inmunogenicidad de los neoantígenos, incluyendo aquellos despreciados por las propias células del paciente en condiciones in vivo. Sin embargo, los linfocitos T de donantes sanos no eran sensibles a todos los neoantígenos candidatos. Los investigadores demostraron que la tasa de éxito de neoantígenos candidatos (es decir, el éxito de predicción de neoantígenos capaces de inducir una respuesta inmune) se mejora con estimaciones de la estabilidad de unión entre los péptidos y el complejo mayor de histocompatibilidad
El estudio es un recordatorio de que se pueden obtener ideas desde sistemas experimentales accesibles y contraintuitivos, en este caso, la sangre periférica de personas sanas. Los repertorios de células T de múltiples donantes pueden utilizarse para estudiar las propiedades que definen un neoantígeno inmunogénico. Los linfocitos T derivados de donantes son activados por epítopes anómalos que vuelan bajo el radar de la inmunidad alterada del paciente. Este hallazgo abre posibilidades de una nueva generación de inmunoterapias a través de la introducción genética de TCR derivados de individuos sanos específicos para los neoantígenos en las células T de un paciente mediante la transferencia adoptiva.
Fuente bibliográfica
The Antigenicity of the Tumor Cell — Context Matters
Vessela N. Kristensen, Ph.D.
Department of Clinical Molecular Biology (EpiGen), Medical Division, Akershus University Hospital, Lørenskog, Oslo, Norway.
DOI: 10.1056/NEJMcibr1613793
Temas Relacionados