Trasplante de macrófagos para la proteinosis alveolar pulmonar
La terapia de la proteinosis alveolar pulmonar (PAP) depende de la progresión de la enfermedad, las infecciones coexistentes y el grado de deterioro fisiológico. El estándar de manejo es la eliminación mecánica del material lipoproteico por lavado pulmonar total. Históricamente, los pacientes han sido tratados con esteroides sistémicos, mucolíticos (aerosol) y proteinasas (aerosol), sin mucho éxito. Por otra parte, en recientes estudios, en la PAP autoinmune, se ha observado que el uso terapéutico del factor estimulante de colonias de granulocitos y macrófagos (GM-CSF), ya sea de forma inhalada o sistémica, ha demostrado ser seguro y eficaz para proporcionar un efecto terapéutico sostenido.
Proteinosis alveolar pulmonar y el trasplante de macrófagos
Los macrófagos son muy variables, y su ontogenia y función dependen del órgano en el que residen y de los procesos de la enfermedad en curso. A su vez, son de importancia crítica para la función pulmonar, y el conocimiento de su morfogénesis y fenotipo se expande rápidamente. Están presentes dentro de los espacios alveolares y en la pared de las vías respiratorias y el lumen. Los macrófagos de las vías respiratorias pueden ser unidades alveolares que están en camino a lo largo de la estructura mucociliar hacia distintas zonas de la nasofaringe, otros tipos tienen su propia ontogenia y función. En pulmones sanos, las funciones generales incluyen servir como un sistema de vigilancia de defensa del huésped para proteger a los pulmones, la modulación de respuestas inflamatorias e inmunes, y la supervisión y regulación de la capa surfactante, que es fundamental para el mantenimiento de una baja tensión superficial, y permitir la apertura de los alvéolos en cada respiración.
En la enfermedad, los macrófagos pulmonares desempeñan papeles muy variados. Pueden iniciar respuestas inflamatorias contra los gases, partículas y amenazas microbianas, facilitar las reacciones inmunes inflamatorias e innatas, y participar en las reacciones fibróticas o granulomatosas que resultan de la remodelación alveolar o de las vías respiratorias y de los defectos de la función pulmonar.
La capa de revestimiento tensioactivo alveolar está estrecha y continuamente regulada por medio de la producción de fosfolípidos y proteínas surfactantes y por las células epiteliales alveolares tipo II y por medio de macrófagos alveolares. La señalización celular iniciada por el receptor del factor estimulante de colonias de granulocitos y macrófagos (GM-CSF) es crítica para la descomposición del surfactante. La proteinosis alveolar pulmonar (PAP) es causada por la señalización defectuosa del receptor de GM-CSF, por lo general debido a una deficiencia genética que produce una menor expresión o función de las subunidades α o β del receptor de GM-CSF o, más comúnmente, o por autoanticuerpos contra GM-CSF, resultando un aclaramiento defectuoso de la lipoproteína surfactante desde el espacio alveolar. El tejido pulmonar distal se llena masivamente con muchos macrófagos alveolares capaces de ingerir el surfactante pero incapaces de procesarlo. En última instancia, disminuyen los resultados de intercambio gaseoso lo que provoca insuficiencia respiratoria hipoxémica y defectos en la defensa del huésped. La enfermedad humana es muy similar- tanto estructural como fisiológicamente - a la deficiencia del receptor de GM-CSF en ratones, un modelo de enfermedad generada por medio del knockout de Csf2rb, que codifica la subunidad β de GM-CSF.
Veronika Kleff y colegas (Mol Ther 2008; 16: 757-64) encontraron que la reconstitución de la médula ósea de estos ratones con células madre hematopoyéticas Csf2rb -/- diseñadas genéticamente para expresar el receptor GM-CSF de ratón revertía completamente la acumulación patológica de surfactante a las 12 semanas, a pesar de los bajos niveles de transducción de 10 a 20% (es decir, sólo una pequeña fracción de células del donante expresaba el constructo). Desarrollaron una proteinosis alveolar pulmonar en ratones y reemplazaron la proteína GM-CSF con la proteína humana GM-CSF, ya que esta última no es reconocida por el receptor de GM-CSF de ratón. El fenotipo de este modelo de PAP mejoró cuando la médula ósea de los animales se reconstituyó con células CD34+ humanas (macrófagos diferenciados). Estos estudios muestran que la sustitución con macrófagos derivados de médula ósea funcional restaura la homeostasis surfactante. Pero en seres humanos, la morbilidad y mortalidad de la ablación de la médula ósea y del trasplante limitan su utilidad.
La posibilidad de trasplantar macrófagos, tal vez después de manipularlos genéticamente, mediante su introducción directa en los pulmones de un paciente, y por lo tanto reparar la lesión pulmonar, ha sido durante mucho tiempo un importante objetivo. El enfoque combinado célula-gen tiene la ventaja de beneficiar a los pacientes con una amplia gama de condiciones pulmonares, incluyendo a la PAP hereditaria (fig. 1). Tres estudios se han acercado a este objetivo, al menos en pacientes con tal enfermedad. Christine Happle y colaboradores (Sci Transl Med 2014; 6: ra113) trasplantaron progenitores de macrófagos derivados de médula de ratón tipo salvaje a las vías respiratorias de ratones Csf2rb -/-, encontrando que estos progenitores revocaban los fenotipos de la proteinosis alveolar pulmonar, lo que sólo se detectaba en pulmones de 5 semanas a 9 meses después del trasplante. En segundo lugar, en el otro modelo de proteinosis alveolar pulmonar, los ratones humanizados que expresaban la interleucina-3 y genes GM-CSF humano, se trataban de manera más efectiva mediante trasplante intrapulmonar de células derivadas de unidades CD34+ aisladas de sangre de cordón umbilical humano.
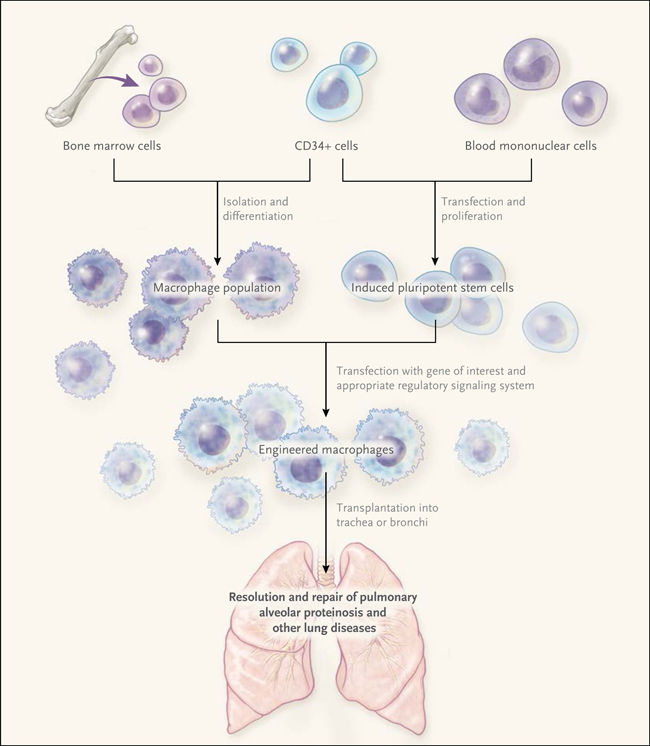
Figura 1: potencial vía para el trasplante de macrófagos
Este esquema implica el aislamiento y diferenciación de los macrófagos a partir de células de médula ósea CD34+. Alternativamente, las células madre pluripotentes inducidas podrían ser generadas de unidades mononucleares de sangre o de células de médula ósea CD34+. Estos macrófagos o células madre pluripotentes inducidas podrían ser transfectadas con el gen o genes de interés y un apropiado sistema de señalización reguladora. En el caso de la proteinosis alveolar pulmonar, la transfección con CSF2RB sería probablemente más eficaz. Estos macrófagos podrían ser trasplantados en la tráquea o en áreas proximales o distales de los bronquios por medio de la visualización broncoscópica de las vías respiratorias y de la instilación. El tratamiento eficaz dependerá de injerto de estas células modificadas.
En tercer lugar, Takuji Suzuki y co-investigadores (Nature 2014; 514: 450-4) encontraron que el trasplante de médula ósea, de tipo salvaje, con macrófagos maduros altamente purificados, en pulmones de ratones Csf2rb -/- resultaba en la proliferación de estos macrófagos, la sustitución de macrófagos alveolares Csf2rb -/-, y la reversión de la enfermedad pulmonar. Además, la progenie de tales macrófagos estaba presente en pulmones de 1 año después del trasplante. Ellos también encontraron que el trasplante de macrófagos Csf2rb -/- derivados de médula ósea revertía la PAP en ratones Csf2rb -/-. Los macrófagos tipo salvaje y Csf2rb corregidos perdieron las características de los macrófagos de médula ósea y ganaron las de los macrófagos pulmonares de tejidos, un hallazgo que era consistente con observaciones anteriores de que el microambiente pulmonar es crítico para determinar el fenotipo y la función de los macrófagos. Estos estudios sugieren que la corrección génica y los macrófagos derivados de médula ósea representan una potencial intervención terapéutica para los pacientes con la forma hereditaria de la proteinosis alveolar pulmonar. Ya se han generado células madre pluripotentes inducidas corregidas genéticamente en determinados pacientes.
Por consiguiente, se puede justificar un ensayo clínico de trasplante de macrófagos pulmonares en individuos con PAP. Hay muchas posibilidades que esta terapia génica de células sea beneficiosa. Los macrófagos que son genéticamente diseñados para regular el estrés oxidativo o la degradación enzimática pueden servir con fines terapéuticos. Se podría imaginar un trasplante de macrófagos que expresen genes que codifiquen proteínas con capacidad de modificar el tejido fibrótico en la enfermedad pulmonar intersticial o la fibrosis pulmonar. Los macrófagos diseñados para inhibir las proteasas o para secretar materiales de la matriz o de estructuras de construcción pueden ser valiosos en patologías como el enfisema. Los macrófagos que poseen canales iónicos capaces de modular la hidratación de la vía aérea pueden ser útiles en muchas afecciones (por ejemplo, bronquitis crónica y fibrosis quística) en el que las anormales propiedades viscoelásticas del esputo alteran las respuestas epiteliales y la defensa del huésped. El enfoque actual de los exosomas de la vía aérea (vesículas derivadas de células que pueden transferir genes y proteínas a partir de un tipo de célula a otra) posibilitaría que los macrófagos modificados para expresar el ARN mensajero del gen que codifica el regulador de la conductancia transmembrana de la fibrosis quística (CFTR) puedan ser utilizados para tratar pacientes con fibrosis quística. Dicho todo esto, es necesario ser cautelosos: su vida útil y su capacidad para proliferar y alterar la homeostasis pulmonar genera preocupaciones sobre la seguridad. En suma, son muchas las oportunidades para el trasplante de macrófagos pulmonares y son dignos de una mayor investigación.
Fuente bibliográfica
Pulmonary Alveolar Proteinosis and Macrophage Transplantation
Claire M. Doerschuk, M.D.
Marsico Lung Institute, Division of Pulmonary Disease and Critical Care Medicine, Department of Medicine, University of North Carolina, Chapel Hill.
DOI: 10.1056/NEJMcibr1413035