El origen de la estenosis aórtica calcificada
¿Cómo dan lugar los estímulos patológicos a la fibrosis y al desarrollo de nódulos calcificados, que comprometen la integridad biomecánica de la válvula aórtica y conducen a la estenosis? Un nuevo modelo experimental animal subraya la necesidad de comprender mejor cómo las vías críticas de las primeras etapas de desarrollo contribuyen finalmente a la afección cardiovascular.
Los mecanismos de la enfermedad de las válvulas cardíacas a menudo imitan los procesos observados en el desarrollo embrionario y de la primera infancia, como la activación de los fenotipos de células intersticiales valvulares (VIC) y la remodelación de la matriz extracelular. Esta reprogramación del desarrollo en la válvula aórtica probablemente representa un intento para reparar el tejido dañado y restaurar la función normal; sin embargo, las respuestas de remodelación son notoriamente pobres en tejidos adultos más inactivos. La persistencia de estímulos patológicos da como resultado la acumulación de colágeno fibrótico y de nódulos calcificados, que comprometen la integridad biomecánica de la válvula aórtica y conducen a la estenosis.
Un estudio reciente acaba de demostrar la relevancia de un particular proceso de desarrollo, la transición endotelial a mesenquimal, en la remodelación patológica de la válvula aórtica (figura 1). Este proceso es clave durante el crecimiento de la válvula cardíaca cuando las células endocárdicas que recubren el tracto de salida y las almohadillas cardíacas migran hacia el tejido subyacente y pueblan las cúspides de la válvula aórtica con VIC. Las unidades que permanecen en la superficie y recubren las cúspides de la válvula aórtica madura se conocen como células endoteliales de válvula (VEC). Las VEC y VIC trabajan en conjunto para mantener la estructura y función de la válvula aórtica. En respuesta a la interrupción de la comunicación entre ambas, la activación de la transición endotelial a mesenquimal hace que las VEC adopten un fenotipo condroosteogénico asociado con la calcificación de la válvula aórtica. Los autores muestran que las VEC condroosteogénicas que experimentan una transición endotelial a mesenquimal derivan de un linaje genético específico que expresa el factor de transcripción de unión a octámero 4 (OCT4, también conocido como POU5F1), que promueve un fenotipo de células progenitoras. Las células positivas para OCT4 se asocian con la calcificación en válvulas aórticas humanas enfermas, y su aumento de expresión conduce a la elaboración de citoquinas proinflamatorias que promueven la transición endotelial a mesenquimal. Una vez que las células de linaje OCT4 migran a las cúspides, expresan genes procalcificantes, participando activamente en la calcificación. La eliminación genética de OCT4 redujo la calcificación y previno la estenosis aórtica en ratones hipercolesterolémicos, lo que demuestra una relación causal entre estos mecanismos de transición endotelial a mesenquimal y la remodelación patológica. Más allá de implicar un potencial beneficio terapéutico al dirigirse a la señalización asociada con OCT4, estas observaciones realzan la necesidad de revisar las vías de desarrollo en el inicio y la progresión de la estenosis aórtica calcificada.
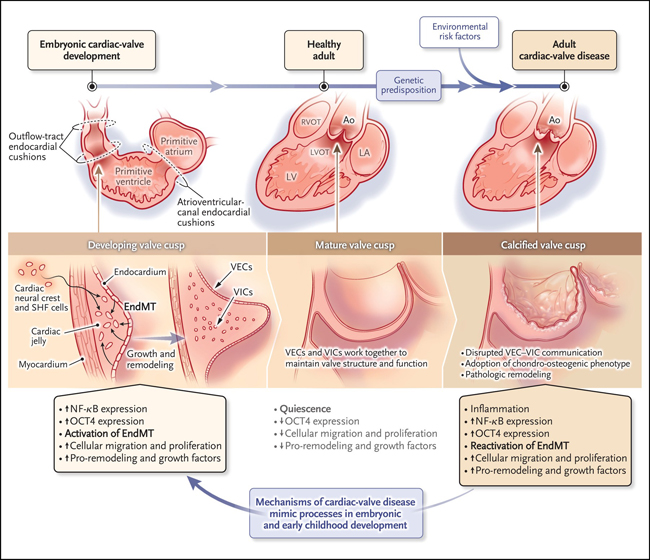
Figura 1: posible efecto de los mecanismos de desarrollo en la estenosis aórtica calcificada.
La reactivación de los mecanismos de desarrollo puede desempeñar un papel fundamental en la remodelación del tejido valvular y conducir a la estenosis aórtica. Los factores de riesgo genéticos predisponen al desarrollo de enfermedad valvular cardíaca calcificada, y los factores de riesgo ambientales modificables contribuyen al inicio y gravedad de la condición. Ao: aorta, EndMT: transición endotelial a mesenquimatosa, LA: aurícula izquierda, LV: ventrículo izquierdo, TSVI: tracto de salida del ventrículo izquierdo, NF-κB: factor nuclear κB, OCT4: factor de transcripción de unión a octámero 4, TSVD: tracto de salida del ventrículo derecho, SHF: segundo campo cardíaco, VEC: células endoteliales de la válvula y VIC: células intersticiales de la válvula.
Varios linajes de desarrollo colaboran al desarrollo de la válvula aórtica, generando una heterogeneidad celular única, compleja y subestimada. Además de la transición endotelial a mesenquimal, las células de la cresta neural y del segundo campo cardíaco pueblan las valvas en desarrollo. Las alteraciones en las contribuciones relativas de estos linajes durante el crecimiento fetal pueden cambiar la estructura de la válvula y provocar malformaciones como las válvulas aórticas bicúspides. La estratificación de distintos patrones de expresión de genes y proteínas en cúspides maduras, y patrones alterados en valvas enfermas, sugiere que poblaciones específicas de células mantienen la microarquitectura extracelular que dicta la función de la válvula. Sin embargo, sigue sin estar clara la contribución exacta de cada uno de los tres linajes embrionarios descritos previamente a los fenotipos celulares y el patrón de matriz extracelular en las cúspides de la válvula aórtica madura y la remodelación asociada en la enfermedad. Se necesita saber más sobre el linaje temporal y de los análisis basados en células individuales desde el embrión hasta la enfermedad de inicio en la edad adulta para mapear los efectos del desarrollo a la homeostasis y remodelación de la válvula aórtica.
Respecto a las válvulas, los estudios de desarrollo y enfermedad han existido con mayor frecuencia como disciplinas separadas, pero los análisis holísticos que unifican el desarrollo, la maduración y la enfermedad valvular podrían conducir a nuevos enfoques para el manejo y tratamiento de la estenosis aórtica. La realización clínica de terapias no invasivas requerirá la identificación de los pacientes antes de que ocurra una remodelación macroscópica, y los procedimientos de reemplazo de válvulas se están probando en estudios para determinar si pueden proporcionar un mayor beneficio si se realizan antes de la enfermedad, antes de que la función cardíaca se vea comprometida de manera irreversible. En muchos pacientes, la manifestación de los síntomas ocurre solo en la estenosis severa, limitando las opciones clínicas que podrían preservar la función cardíaca y reducir futuras complicaciones. Las disparidades socioeconómicas y raciales de síntomas como fatiga y disnea también pueden contribuir a ampliar las diferencias en los resultados de los pacientes con estenosis aórtica, ya que las nuevas directrices e intervenciones requieren una identificación más temprana de la enfermedad. El reconocimiento de que los factores de desarrollo y la reactivación de las vías de desarrollo pueden contribuir a la estenosis aórtica podría proporcionar una nueva perspectiva de los riesgos individuales de la remodelación de válvulas. Los análisis familiares señalan una fuerte contribución genética al riesgo de estenosis aórtica. Se ha encontrado que las personas con al menos un hermano con estenosis aórtica tienen un riesgo significativamente mayor de desarrollar enfermedad de la válvula aórtica que aquellas que no la tienen (índice de riesgo, 3,4; intervalo de confianza [IC] del 95 %, 2,2 a 5,2). Se sabe que el riesgo asociado aumenta aún más cuando dos o más hermanos padecen estenosis aórtica (razón de riesgo, 32,8; IC del 95 %, 20,5 a 65,2), mientras que el riesgo asociado con un diagnóstico de estenosis del cónyuge es modesto (razón de riesgo, 1,2; 95 % % IC, 1,1 a 1,3). En algunos individuos, la reaparición de mecanismos de desarrollo en la enfermedad puede reflejar una predisposición genética a la remodelación de la válvula aórtica en la adultez. Una nueva visión mecánica de las conexiones entre el desarrollo de la válvula aórtica y la enfermedad podría conducir a una reevaluación de la evaluación del riesgo individual y el posterior manejo de la estenosis aórtica.
Fuente bibliográfica
The Developmental Origin of Calcific Aortic Stenosis
E. Aikawa and J.D. Hutcheson
Brigham and Women’s Hospital and Harvard Medical School, Boston (E.A.); and Florida International University, Miami (J.D.H.).
N Engl J Med 2022; 386:1372-1374