El ingenio tumoral para alcanzar la inmortalidad
La reparación del ADN mediante recombinación homóloga es esencial para el mantenimiento del genoma. Un mecanismo molecular, conocido como alargamiento alternativo de los telómeros (ALT) requiere la restauración de secuencias de ADN para mantener los extremos de cromosomas en aproximadamente el 10 - 15% de las células tumorales humanas. Sin embargo, la forma en que el daño del material genético induce el ensamblaje y ejecución de un complejo de replicación en los telómeros o en otras partes del genoma de mamíferos es poco conocido. Recientes estudios definen la síntesis de telómeros que es inducida por quiebres en la doble hebra del ADN y evidencian un mecanismo que utiliza proteínas especializadas que subyacen al mantenimiento de telómeros tipo ALT. Estos hallazgos podrían contribuir a entender cómo se inicia el ALT y cómo es mantenido en células tumorales humanas, lo que permitirá en el futuro poder desarrollar terapias dirigidas al cáncer.
Alargamiento de telómeros
Durante la división celular, el genoma es duplicado por enzimas llamadas ADN polimerasas. Sin embargo, los extremos de cada cromosoma no se replican completamente durante la duplicación del material genético, porque las ADN polimerasas requieren una corta secuencia iniciadora (cebador) de ARN con un extrmo 5' para la regíon que se necesita sintetizar. Esto significa que las secuencias repetitivas de ADN como los telómeros que cubren los extremos de los cromosomas se acortan con cada división celular, y este acortamiento limita la vida replicativa de la mayoría de las células. Durante el desarrollo del cáncer, las células adquieren la capacidad de dividirse indefinidamente, mediante la elusión del acortamiento del telómero - ya sea por regulación positiva de la enzima telomerasa, que extiende los telómeros, o por la activación de un mecanismo denominado alargamiento alternativo de telómeros (ALT), que se basa en un método de reparación del ADN: la recombinación homóloga. En un reciente estudio Robert L. Dilley y colaboradores revelaron un mecanismo que subyace a ALT e identificaron una inusual ADN polimerasa que media este proceso.
Durante la recombinación homóloga, un quiebre en la doble hebra del ADN de un cromosoma es reparado por una ADN polimerasa utilizando un molde o templado que se toma de una cromátida hermana - un molécula de ADN idéntica generada durante la replicación. Las células cancerosas que usan ALT a menudo muestran mayores niveles de daño en el ADN telomérico, lo que puede predisponerlas a utilizar la recombinación homóloga para reparar las roturas en estas regiones del genoma. En líneas celulares de cáncer humano que utilizan el mecanismo ALT, existe evidencia de recombinación en telómeros que incluye un aumento de los intercambios de telómeros entre cromátidas hermanas. Un total aproximado de 10 - 15% de los tumores utilizan ALT para mantener sus telómeros, haciendo uso de este proceso, lo que genera una oportunidad para implementar terapias anticancerígenas a ese nivel. Sin embargo, la determinación exacta de los mecanismos moleculares implicados en el ALT ha sido un gran desafío.
Hay dos maneras en que los telómeros pueden utilizar recombinación homóloga para mantener su longitud. En el primer modelo, un desigual intercambio de ADN entre telómeros hermanos crea un telómero más largo y otro más corto, uno de los cuales es heredado por cada célula hija. Las células que heredan telómeros más largos eventualmente superan a las que tienen menor extensión de estas estructuras. En el segundo modelo, que está ganando cada vez más favor, el ADN telomérico se sintetiza usando una pieza existente de templado telomérico, ya sea de otro telómero o de moléculas libres de ADN repetitivo llamadas ADN telomérico extracromosómico que se encuentran en células ALT.
Dilley y colegas dieron un fuerte apoyo al segundo modelo. Para fomentar la recombinación homóloga en células ALT, los autores explotan un sistema que habían diseñado anteriormente para crear quiebres de doble hebra, dirigidos a telómeros, mediante fusión de la enzima nucleasa Fok1, que corta el ADN, con la proteína de unión a telómeros TRF1. Observaron un aumento de diez veces en la síntesis de ADN telomérico después de la inducción de TRF1-Fok1 en células conocidas por utilizar ALT. Además, mostraron que esta síntesis es unidireccional y procesiva - capaz de sintetizar largas extensiones de telómeros repetidos, típicamente 20 kilobases (longitud promedio de un telómero ALT).
Las características y la cinética de esta síntesis de ADN coinciden con la de un fenómeno llamado replicación inducida por rotura, que es un mecanismo de mantenimiento de telómeros en cepas de levaduras que carecen de telomerasa. Este método es una forma de recombinación homóloga que inicia la replicación del ADN cuando sólo un extremo de un quiebre en la doble hebra comparte similaridad de secuencia (complementaridad de bases) con un templado. Los investigadores llamaron a este proceso (en células de mamíferos que sufren ALT) “síntesis de telómeros inducida por quiebre”.
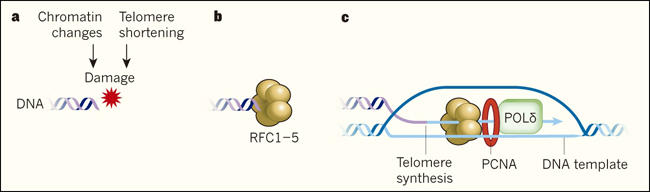
Figura 1: Síntesis de telómeros inducida por quiebre.
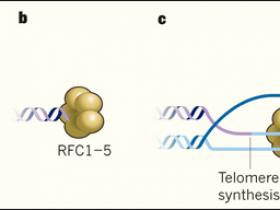
Algunas células cancerígenas mantienen las secuencias de ADN teloméricas a través de un mecanismo denominado alargamiento alternativo de telómeros (ALT). Dilley y sus colegas, describieron un proceso llamado síntesis de telómeros inducido por rotura, que subyace al ALT. a, Las rupturas de ADN de doble hebra pueden surgir en los telómeros por varias razones, como por el acortamiento de estas estructuras durante la división celular o por cambios en la forma en que el ADN telomérico se empaca como cromatina.b, En las células ALT, el complejo de proteínas RFC1-5 se une rápidamente a las roturas de doble hebra en los telómeros. c, RCF1-5 recluta la proteína PCNA y a la enzima ADN polimerasa POL δ, hacia el sitio de la ruptura. Este complejo proteico sintetiza largas extensiones de ADN usando una cadena complementaria de ADN como una plantilla a partir de la que replica el telómero.
Posteriormente, los autores caracterizaron las proteínas responsables de la síntesis inducida por quiebre. La proteína Rad51 tiene un papel clave en la recombinación homóloga, y se requiere para la replicación inducida por rotura en levaduras. Pero, sorprendentemente, se observó que Rad51 era prescindible en células ALT. Más bien, un complejo consistente en la polimerasa POLδ y las proteínas PCNA y RFC1-5 se encontró en los sitios del daño en el ADN en estas células y se determinó que eran requisitos para la síntesis (figura 1).
Sin embargo, aún no está claro qué es lo que induce el mecanismo ALT y cómo puede sostenerse específicamente en el 10 a 15% de los tipos de células cancerosas que utilizan ALT. Los autores proporcionan una posible explicación: las células ALT tienen mayores tasas de daño persistente en sus telómeros que otras células cancerosas.
Finalmente, la investigación proporciona evidencia que podría ayudar a entender mejor cómo el ALT se inicia y se mantiene en células tumorales humanas. En el futuro, una comprensión de estos procesos podría conducir al desarrollo de terapias dirigidas a cánceres que dependen de ALT para progresar.
Fuente bibliográfica
DNA repair: Telomere-lengthening mechanism revealed
Caitlin M. Roake and Steven E. Artandi
Departments of Medicine and of Biochemistry and the Cancer Biology Program, Stanford University School of Medicine, Stanford, California 94305, USA.
doi:10.1038/nature19483