Adipocitos con un gusto por lo dulce
Las señales ambientales afectan profundamente la plasticidad celular en los organismos multicelulares. Por ejemplo, el ejercicio promueve un cambio de tipo de fibra glucolítica a oxidativa en el músculo esquelético, y la aclimatación al frío induce biogénesis de adipocitos beige en el tejido adiposo. Sin embargo, los mecanismos moleculares por los cuales las señales fisiológicas o patológicas evocan la plasticidad permanecen incompletos. Recientemente, se ha documentado un tipo de adipocito beige que tiene un papel crítico en la adaptación al frío crónico en ausencia de señalización del receptor β-adrenérgico. Esta grasa se diferencia de la beige convencional en cuanto a su origen y regulación del desarrollo, y muestra una mayor oxidación de la glucosa. Por lo tanto, se refiere a ella como grasa glucolítica beige. El estudio revela un mecanismo de adaptación no canónico por el cual el estrés térmico induce plasticidad de las células progenitoras y recluta una forma distinta de célula termogénica que es necesaria para la homeostasis energética y la supervivencia.
Adipocitos beige especiales
A menudo se piensa que la grasa es un medio para almacenar energía en forma de lípidos. Pero esto es sólo el papel de las células de la grasa blanca. El cuerpo también contiene un segundo tipo de grasa que "quema" la energía almacenada en los nutrientes para producir calor, permitiendo a los mamíferos mantener su temperatura corporal en un ambiente frío. Se cree que la activación de esta grasa "termogénica" es una forma atractiva de combatir la obesidad. Recientemente, Chen y cols. (DOI: 10.1038/s41586-018-0801-z) identificaron un tipo de célula grasa termogénica no caracterizada anteriormente, que se deriva de un linaje celular hasta ahora desconocido y que metaboliza principalmente azúcar, en lugar de la combinación usual azúcar y lípidos, procesada por la mayoría de la grasa termogénica. Su descubrimiento podría abrir nuevas posibilidades terapéuticas para la pérdida de peso.
Las células grasas termogénicas se clasifican actualmente como parda o beige. A diferencia de la grasa parda, las células grasas beige se encuentran entremezcladas en la grasa blanca. La producción de adipocitos beige puede desencadenarse en respuesta al frío mediante la activación de receptores β-adrenérgicos en la superficie de las células precursoras en los depósitos de tejido graso blanco. Estos receptores son estimulados por la vía de señalización β-adrenérgica, que se origina en el sistema nervioso.
Se han hecho grandes esfuerzos para tratar la grasa termogénica para la pérdida de peso, pero hasta ahora no se ha desarrollado ningún fármaco exitoso. Esto se debe en parte al hecho de que la cantidad de grasa parda activa varía entre los individuos y disminuye con la edad. Además, las estrategias actuales para inducir la formación y activación de la grasa beige típicamente involucran la simulación de respuestas al frío, y se cree que actúan a través de la señalización β-adrenérgica. Esto afecta inevitablemente a otros órganos, porque los receptores β-adrenérgicos se expresan ampliamente a través de varios tejidos - y tal falta de especificidad plantea problemas de seguridad. Por lo tanto, otras formas de inducir la formación y activación de la grasa termogénica serían muy valiosas.
Chen y cols. se propusieron identificar vías alternativas para activar la grasa termogénica utilizando un modelo animal llamado ratón β-menos, que carece de los tres receptores β-adrenérgicos. Confirmaron estudios previos de que algunas células grasas beige todavía se producían en estas condiciones (figura 1).
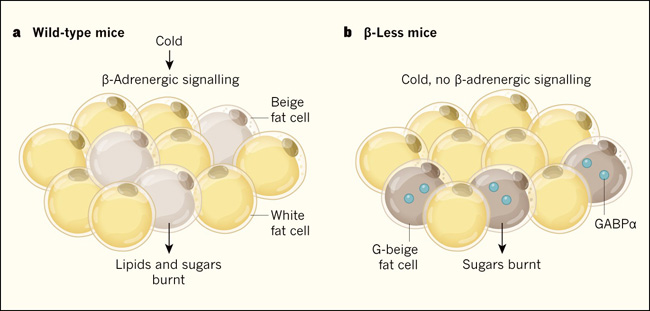
Figura 1. Vías duales para producir adipocitos generadores de calor.
a, Las células de grasa blanca almacenan energía. En ratones silvestres, en condiciones frías, los receptores β-adrenérgicos en las células precursoras de adipocitos (no mostradas) son activados por una vía de señalización que permite la diferenciación de algunos precursores celulares en células de grasa beige, en los tejidos de grasa blanca. Estos adipocitos beige consumen energía de los lípidos y del azúcar para liberar calor, manteniendo la temperatura corporal. b, Chen y cols. (DOI: 10.1038/s41586-018-0801-z) analizaron ratones sin receptores β-adrenérgicos (β-Less mice) lo que implica que la señalización mediada por estos receptores se bloquea. Los autores demostraron que un tipo diferente de grasa beige, denominada grasa beige glucolítica (g-beige fat), surge en estos animales en condiciones de frío. La diferenciación de estas células a partir de un grupo de precursores que expresan la proteína precursora muscular MyoD (no mostrada) está impulsada por el factor de transcripción GABPα.
¿De dónde vienen estas células? Chen y sus cols. realizaron una caracterización en profundidad de la expresión génica en los tejidos grasos de ratones β-menos, lo que reveló que los genes implicados en el desarrollo muscular se expresaban más en los tejidos grasos que carecían de receptores β-adrenérgicos que en los de los animales control. Los autores diseñaron genéticamente ratones para que las células que expresan uno de estos genes, Myod (que codifica la proteína MyoD y se expresa normalmente en precursores de células musculares), fueran marcadas con una proteína fluorescente. Luego bloquearon la señalización β-adrenérgica usando un medicamento y expusieron a los ratones a un frío leve, antes de rastrear el destino de las células que expresan MyoD y sus descendientes. Este experimento de rastreo de linaje reveló que algunas células que expresan MyoD dan lugar a un subconjunto de células grasas beige, lo que sugiere que los precursores de células musculares pueden ser reprogramados para convertirse en células grasas beige específicas.
Cuando analizaron los perfiles de expresión génica de las células, los autores encontraron que este subconjunto de grasa beige difiere del de la grasa beige convencional. El subconjunto expresa niveles más altos de muchos genes implicados en la glucólisis y el metabolismo de hidratos de carbono. Sobre la base de este perfil, los autores las apodaron células grasa beige glucolíticas (grasa g-beige). Los datos indicaron que el factor de transcripción GABPα impulsa la diferenciación de los progenitores que expresan MyoD en células grasas g-beige. Los autores confirmaron esta suposición in vitro, mostrando que la sobreexpresión de GABPα en los progenitores musculares lleva a su diferenciación en adipocitos.
También demostraron que la grasa g-beige tiene un papel fisiológico en ratones, principalmente quemando azúcar para producir calor. La grasa g-beige se generó en animales silvestres sometidos a condiciones de frío prolongado e intenso. Además, los animales diseñados para no producir grasa g-beige mostraron una menor asimilación de glucosa y consumo de oxígeno en comparación con los controles; su capacidad para controlar la temperatura corporal en respuesta al frío también se vio afectada.
Los hallazgos de los autores son emocionantes por varias razones. En primer lugar, este estudio refuerza la idea de que la grasa madura está compuesta de varios tipos de células. Es plausible que existan otras subpoblaciones de células grasas parda, beige e incluso blancas. Estos tipos de células podrían tener diferentes funciones en la regulación del metabolismo de todo el cuerpo. Además, es posible que las células grasas g-beige tengan otras funciones además de la termogénesis. Por ejemplo, en los últimos años se ha hecho evidente que la grasa parda se comunica con otros tejidos mediante la secreción de moléculas de señalización específicas -quizás la grasa g-beige modula de forma similar la señalización hormonal en el cuerpo para promover la comunicación cruzada con otros tejidos.
En segundo lugar, la grasa g-beige se induce a través de una vía previamente desconocida, que podría estar dirigida específicamente a mejorar el control glucolítico, un factor clave en el tratamiento de la diabetes tipo 2. Y si estas células también están presentes en los seres humanos, su caracterización podría allanar el camino para nuevos enfoques de activación de las células grasas termogénicas. Para que tales enfoques tengan éxito, los investigadores primero necesitarían determinar cómo se induce la grasa g-beige, incluyendo qué receptores y cascadas de señalización subsecuentes desencadenan la diferenciación mediada por GABPα. A la luz de la actual epidemia de obesidad, se requieren enfoques eficientes y seguros para regular el exceso de peso corporal. El descubrimiento de la grasa g-beige podría ser una forma de hacerlo.
Fuente bibliográfica
Fat cells with a sweet tooth
Wenfei Sun & Christian Wolfrum
Institute of Food, Nutrition and Health, ETH Zurich, 8603 Schwerzenbach, Switzerland.
DOI: 10.1038/d41586-018-07739-6