Suplementos antioxidantes: combustible para el cáncer
Los antioxidantes son compuestos químicos producidos por plantas y se encuentran preferentemente en frutas, verduras, legumbres y granos. Debido que comer una gran variedad de alimentos de origen vegetal proporciona muchos beneficios de salud, incluyendo la reducción del riesgo de cáncer, algunos especulan que ingerir suplementos de antioxidantes podría ayudar a prevenir muchas enfermedades. Sin embargo, la evidencia científica no ha sido capaz de demostrar que tan bueno son para la salud a largo plazo cuando se consumen frecuentemente.
Algunos de los más conocidos son el beta caroteno, el ácido ascórbico (vitamina C) y la vitamina E. La mayoría de los estudios con antioxidantes han decepcionado a los investigadores quienes tenían la esperanza de encontrar una fuente inagotable para la lucha contra una variedad de condiciones. Por ejemplo, los estudios han demostrado que tomar grandes cantidades de vitamina E no sólo no previene el cáncer de próstata, sino que en realidad puede aumentar su riesgo. Otros ensayos han observado una relación directa entre el beta caroteno y el cáncer de pulmón.
Antioxidantes en pacientes con cáncer
Se ha propuesto que las especies reactivas de oxígeno (ROS, por sus siglas en inglés), pueden acelerar o retrasar el inicio y la progresión del cáncer. Estos resultados contradictorios se explicarían por las múltiples funciones que desempeñan las ROS durante la evolución de las células cancerosas.
Las ROS promoverían el cáncer mediante la oxidación de restos químicos intracelulares, lo que resulta en mutaciones genéticas y la activación de las vías bioquímicas que estimulan la proliferación y transformación neoplásica. Estas propiedades tumorigénicas de las ROS han llevado a la evaluación de los antioxidantes en la dieta como potenciales agentes preventivos y terapéuticos en modelos animales y en seres humanos. Aunque algunos estudios preclínicos apoyaban este concepto, los antioxidantes dietéticos han fallado en reducir la incidencia de carcinoma en los ensayos clínicos prospectivos realizados en personas. Por el contrario, algunas investigaciones sugieren un efecto perjudicial de los antioxidantes en individuos con situación de riesgo para el cáncer. Un reciente estudio de Volkan I. Sayin y co-investigadores (Sci Transl Med 2014; 6(221):221ra15) realizado en ratones genéticamente modificados para imitar el cáncer de pulmón de células no pequeñas humano ha confirmado que los antioxidantes N-acetilcisteína y vitamina E en realidad elevan la carga de cáncer y la mortalidad en una forma dependiente de la dosis. ¿Por qué han fracasado los antioxidantes para reducir la tasa de carcinoma en los modelos experimentales y en ensayos clínicos? Recientes descubrimientos sobre la biología mecanicista de las ROS proporcionan explicaciones para el fracaso de los antioxidantes cuando se agregan a la dieta de los pacientes.
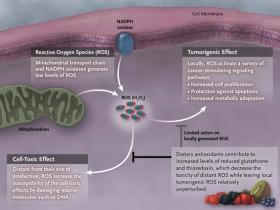
Las ROS juegan un papel importante en la fisiología celular normal, en donde sus bajos niveles se producen a partir del oxígeno molecular a través de la respiración mitocondrial y una familia de NADPH oxidasas unidas a la membrana (NOXS) (fig. 1). Estas ROS oxidan proteínas ubicadas espacialmente para activar múltiples vías de señalización que regulan la viabilidad celular, la proliferación, la diferenciación y la adaptación metabólica. Las células cancerosas aumentan su producción de ROS mitocondrial para estimular aún más la transformación neoplásica. Sin embargo, la respuesta de las células es bifásica: altos niveles de ROS también son tóxicos. En particular, el peróxido de hidrógeno de ROS (H2O2) puede difundir a partes distantes y causar daño oxidativo, deteniendo el ciclo celular y posterior muerte de las células. De hecho, el efecto terapéutico de la radiación ionizante y de muchos agentes quimioterapéuticos comunes en el tratamiento del cáncer depende de la acción citotóxica de las ROS.
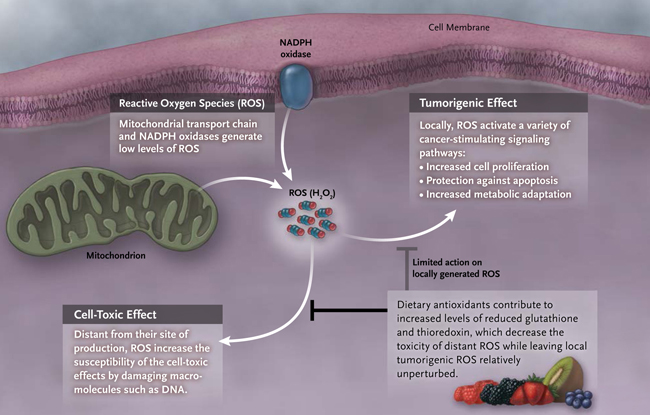
Figura 1: efecto de los antioxidantes de la dieta sobre las especies reactivas de oxígeno (ROS)
Los bajos niveles de ROS son controlados por la cadena mitocondrial transportadora de electrones y por las NADPH oxidasas localizadas en la membrana plasmática y otras membranas de orgánulos. Las ROS generadas en estos sitios oxidan específicamente ciertas proteínas espacialmente yuxtapuestas con la finalidad de activar una variedad de vías de señalización estimuladoras del cáncer. Distante de las mitocondrias y las NADPH oxidasas, las ROS dañan macromoléculas de forma no específica (ADN, ARN, lípidos y proteínas) y son tóxicas para células normales y cancerosas. Los altos niveles de ROS al interior de las células (por ejemplo, a través de la radiación ionizante y la quimioterapia) son tóxicos para las células de manera similar. En comparación con las células normales, las neoplásicas generan más ROS, requiriendo una capacidad antioxidante mayor para controlar el daño, permitiendo simultáneamente la señalización de ROS y la proliferación celular y la supervivencia.
Para compensar los altos niveles intrínsecos de ROS, las células cancerosas han desarrollado mecanismos de adaptación que aumentan las propiedades antioxidantes de las células y por lo tanto mantienen concentraciones reducidas de glutatión y tiorredoxina. Esto permite que utilicen las ROS para activar las vías de señalización proximales, estimulando el comportamiento de células neoplásicas, mientras que de forma simultánea y rápida reparan el daño oxidativo colateral causado por las ROS en diferentes macromoléculas, que de otro modo induciría la muerte o senescencia de las células tumorales.
En base a la comprensión de la biología redox de las células cancerosas, se proponen dos posibles enfoques terapéuticos antioxidantes para prevenir o tratar el cáncer. En primer lugar, las terapias que inhiben directamente la producción mitocondrial y las ROS derivadas de NOX, lo que sería más eficaz que antioxidantes en la dieta. De hecho, los antioxidantes mitocondriales son inhibidores más potentes de la proliferación tumoral que los mismos antioxidantes que se concentran en el citosol. Por lo tanto, el fracaso de la acción de los antioxidantes de la dieta en ensayos clínicos podría ser debido a su incapacidad para secuestrar las ROS en el sitio de producción. Por extensión, las propiedades cancerígenas de los antioxidantes en la dieta siempre son representativas de la estimulación de las proteínas oncogénicas que son atenuadas por ROS distantes, pudiendo reflejar también la inactivación de ciertas proteínas supresoras de tumores, incluyendo p53, que son activadas inversamente por ROS.
En segundo lugar, es posible que exista una estrategia letal que desactive los antioxidantes dentro de las células cancerosas para corregir el daño oxidativo causado por H2O2, permitiendo así la detención celular o la muerte. De hecho, la inhibición genética o farmacológica de las proteínas antioxidantes disminuye la carga tumoral en modelos experimentales de ratón para el cáncer de pulmón y el de páncreas. Un desafío para este enfoque es identificar proteínas antioxidantes y las vías que utilizan de manera selectiva las células cancerosas y células madre específicas, para mantener el equilibrio redox. El perfil antioxidante de las células tumorales y de sus células normales adyacentes puede descifrar las vías antioxidantes que están enriquecidas en las células tumorales como posibles dianas terapéuticas, proporcionando una estrategia adaptada para disminuir la incidencia del cáncer y mejorar los resultados del tratamiento en los pacientes.
Fuente bibliográfica
The Promise and Perils of Antioxidants for Cancer Patients
Navdeep S. Chandel, Ph.D., and David A. Tuveson, M.D., Ph.D.
Feinberg School of Medicine, Northwestern University, Chicago (N.S.C.); and the Lustgarten Foundation Laboratory at Cold Spring Harbor Laboratory, Cold Spring Harbor, NY (D.A.T.).
DOI: 10.1056/NEJMcibr1405701