Beneficios de la inflamación durante la vejez
Recientes estudios en ratones han mostrado que células encargadas de suprimir la respuesta inmunológica, conocidas como linfocitos T reguladores, se acumulan en el tejido adiposo en el curso del envejecimiento. Contrariamente a lo pensado, la actividad antiinflamatoria mediada por estas células, se correlaciona con una desregulación metabólica y con una menor capacidad para que las grasas sean remodeladas, lo cual ocurre en función del avance de la edad pero independiente de la obesidad. Sorprendentemente, al eliminar estos linfocitos acumulados en el tejido adiposo de ratones de edad avanzada, se encontró que estos almacenaban menor contenido graso y mejoraban diversos parámentros metabólicos, tales como la resistencia insulínica y los niveles de glucosa. La depleción de estas células supresoras, se relacionó a un aumento de TNF-α, molécula proinflamatoria por excelencia, revelando que algunos aspectos de la respuesta son beneficiosos a edades tardías. La plena comprensión del rol de estas células en la desregulación metabólica asociada al envejecimiento es fundamental, dado que la edad es un factor de riesgo para patologías metabólicas de alta prevalencia, por lo que potenciales focos terapéuticos dirigidos a tales procesos inmunológicos serían de gran relevancia clínica.
Células supresoras
La grasa corporal sufre una extensa y frecuente remodelación, como cambios en el desarrollo de vasos sanguíneos, en el tejido conectivo, en el número y tamaño de células adiposas y otras características que permiten su almacenamiento o liberación para la obtención de energía requerida por el organismo. Sin embargo, este proceso adaptativo puede llegar a ser perjudicial en condiciones de estrés. La remodelación inadecuada en roedores obesos y en humanos se asocia a una mayor cantidad de células adiposas y a inflamación crónica en zonas grasas, lo que puede llevar a una resistencia insulínica, diabetes tipo 2 y complicaciones cardiovasculares. Los intentos por distinguir los componentes que causan estas alteraciones han revelado un circuito inflamatorio coordinado que implica interacciones entre varios tipos celulares. En un estudio reciente Bapat y colaboradores (Nature. 2015 Nov 18. doi: 10.1038/nature16151) agregaron un nuevo giro a la historia, proporcionando evidencia que, contrariamente a lo que podría esperarse, los cambios metabólicos asociados a la edad pueden ser regulados por mecanismos diferentes de aquellos relacionados a la obesidad.
Células del sistema inmunológico especializadas, llamadas células T reguladoras (células Treg), suprimen la respuesta inflamatoria impulsada por células blancas de la sangre. La importancia de este tipo celular para el funcionamiento del sistema inmunitario se pone de manifiesto por el hecho de que los mamíferos, que carecen del factor transcripcional FOXP3 - el que controla el desarrollo, mantenimiento y función de las células Treg - desarrollan una condición autoinmune multiórgano. Aunque muchas células inmunitarias diferentes están presentes en el tejido adiposo, las células Treg allí residentes (células fTreg) han llamado la atención como moduladores potenciales de la inflamación local.
Las células Treg entran en la grasa inmediatamente después del nacimiento, se acumulan durante el envejecimiento y adquieren un perfil molecular caracterizado por la expresión de varios factores, incluyendo el factor de transcripción PPAR-γ, que controla la diferenciación y la subunidad proteica ST2 (receptor de IL-33), que participa en el desarrollo de las células fTreg . Además, algunos receptores proteicos de células T (que reconocen antígenos durante una respuesta inmunológica) se expresan preferentemente en las células fTreg más que en otras células reguladoras, lo que sugiere que ciertas poblaciones de fTreg proliferaran en contacto con los antígenos. Aunque queda mucho por aprender, la información acerca de modelos de obesidad en animales sugiere que las células fTreg protegen contra la inflamación y la disfunción metabólica.
Bapat y su equipo analizaron células fTreg en el envejecimiento de ratones, en lugar de realizarlo en modelos de obesidad, y modificaron la visión sobre supuestos anteriores relacionados a estas células. El entendimiento de la desregulación metabólica asociada al envejecimiento es vital, porque la edad es un factor de riesgo importante para la resistencia a la insulina y diabetes. Los autores observaron una sorprendente acumulación de células fTreg relacionada a la edad. Pero inesperadamente, cuando los autores eliminaban la población de fTreg mediante la supresión de PPAR-γ en estas células, encontraron que los ratones mutantes ganaban menos peso que sus contrapartes tipo silvestres - acumulaban menos grasa corporal y más peso magro, además comieron y quemaron más calorías que los controles de la misma edad.
Todos los parámetros metabólicos analizados fueron mejor en estos ratones. Los niveles de glucosa e insulina en ayunas disminuyeron, así como también lo hizo la resistencia insulínica. Por el contrario, la expansión farmacológica de la población de fTreg elevó los niveles de esta condición y otros parámetros de desregulación metabólica.
Los investigadores encontraron que el agotamiento de estas células se vinculaba a un aumento de los niveles locales de la molécula pro-inflamatoria TNF-α, consistente con aumento de la inflamación en la grasa corporal. El agotamiento también se correlacionó con una reducción en el tamaño de adipocitos y con una reducción de la expresión génica de colágeno - evidencia de la mejora metabólica de la actividad y remodelación beneficiosa de grasas. Las células fTreg relacionadas al envejecimiento, mantuvieron su perfil molecular y su capacidad de suprimir respuestas inmunológicas, lo que indica que su función no sufrió alteraciones. Estos datos demuestran que la acumulación de fTreg desempeña un rol en la desregulación metabólica asociada a la edad, y que al menos algunos aspectos de la respuesta inflamatoria, la que es suprimida por estas células, son favorables en el envejecimiento (fig. 1).
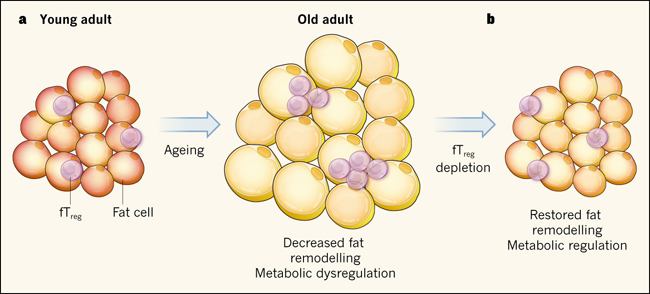
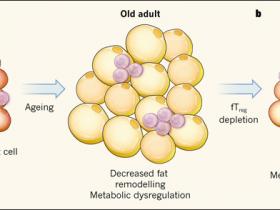
Figura 1: las células T reguladoras afectan la regulación del metabolismo de grasas en ratones de edad avanzada.
a, durante el envejecimiento, las células T reguladoras residentes en tejido adiposo (fTreg) se acumulan en la grasa corporal y disminuyen la inflamación local (rojo). Esta acumulación en función de la edad se correlaciona con aumentos en la desregulación metabólica y en el tamaño de las células adiposas, y con una disminución en la capacidad de la grasa para ser remodelada - proceso por el cual la grasa sufre alteraciones morfológicas en respuesta a las cambiantes demandas de nutrientes. b, Bapat y colegas eliminaron la población celular de fTreg en ratones envejecidos. Este aumento de la inflamación, redujo el tamaño de las células adiposas y mejoró la remodelación de grasa, favoreciendo la regulación metabólica.
Estos sorprendentes resultados contrastan con observaciones anteriores, que indican que el número de fTreg disminuye en ratones obesos, y que la expansión de éstos mejora la salud metabólica sin afectar el peso. A pesar de que este estudio se centró en el envejecimiento, algunos de sus resultados son notablemente divergentes de anteriores hallazgos. Por ejemplo, los autores no encontraron que las células fTreg modularan el metabolismo en un modelo de alto contenido dietario graso en casos de obesidad (aunque había pocas células fTreg en tejido graso y la consecuencias de la expansión de la población celular no fueron probadas en este modelo). Directamente contradiciendo investigaciones anteriores, se encontraron con que al estimular la actividad PPAR-γ con el antidiabético rosiglitazona, se ejercieron efectos metabólicos beneficiosos en ratones obesos, incluso en aquellos donde la actividad de PPAR-γ había sido eliminada, lo que sugiere que otros tipos de células son blancos relevantes de este medicamento.
Las razones de estas discrepancias aún no han sido explicadas. Tal vez estas representan diferencias en el diseño experimental, o de poblaciones de bacterias comensales distintas en los ratones utilizados en ambos estudios. También es de relevancia evaluar si los efectos observados en células fTreg se aplican a los seres humanos. Por otro lado, un factor complejo es que la desregulación metabólica asociada a la obesidad y al envejecimiento a menudo son fenómenos coexistentes.
Sin embargo, la información acerca de las células fTreg y la inflamación va en aumento. En primer lugar, otros laboratorios también han detectado la acumulación de Treg dependiente del envejecimiento, aunque el impacto metabólico de esto no ha sido evaluado. En segundo lugar, está emergiendo una comprensión del perfil de la expresión génica de estas células, ofreciendo pistas sobre su regulación molecular y herramientas que podrían ser utilizadas para manipular sus funciones. En tercer lugar, pruebas convincentes apoyan la existencia de antígenos en tejido adiposo que impulsan la expansión de células fTreg; estos son probablemente presentados a las células mediante el complejo mayor de histocompatibilidad de clase II (MHC II). Por lo tanto, será crucial la identificación de tales antígenos y otros factores que puedan contribuir a la acumulación de células fTreg durante el envejecimiento.
¿Existe la comunicación cruzada entre las células fTreg y otras células inmunitarias, como las células linfoides innatas (CLI)? Reportes recientes, han demostrado que las CLI se infiltran en el tejido graso, indicando que IL-33 activa a CLI 2 para inducir que la grasa blanca se transforme en grasa beige productora de calor. Es posible que IL-33 tenga dos funciones opuestas: la inducción de gasto de energía a través de CLI 2, pero asegurando su conservación a través de la expansión de la población fTreg y mediante la inducción de la secreción de moléculas tales como IL-10 promoviendo actividad anabólica (aumento del almacenamiento de energía en forma de grasa). Por lo tanto, el agotamiento de fTreg podría inclinar el balance a favor del gasto de energía, causando pérdida de peso y mejorarando la salud metabólica. Sin embargo, hasta ahora no se han realizado estudios sobre IL-33 o CLI 2 en ratones envejecidos.
Finalmente, el bloqueo de las vías inflamatorias durante el envejecimiento de células adiposas, se ha relacionado a un deterioro de la regulación metabólica, en contraste con la visión de Bapat y colegas. La identificación de elementos beneficiosos de la respuesta inflamatoria y la investigación de sus efectos metabólicos, será esencial, y podrá apuntar a características conservadas evolutivamente acerca de la inflamación y adaptación del tejido en condiciones anormales. En conclusión, en el tejido adiposo y en otros sitios, las diferentes facetas de la inflamación podrían tener muchos roles, tanto beneficiosos como perjudiciales.
Fuente bibliográfica
Metabolism: Inflammation keeps old mice healthy
Ivan Maillard & Alan R. Saltiel.
University of Michigan, Ann Arbor, Michigan 48109, USA.
doi:10.1038/nature15648