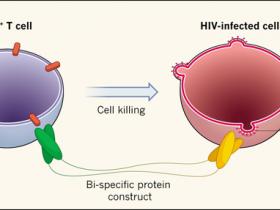
VIH: eliminando células para curar
Uno de los problemas de la infección por VIH es que genera reservorios producto de una infección latente, los que terapias antirretrovirales son incapaces de eliminar por completo. Con el propósito de resolver este gran inconveniente, recientes investigaciones han posibilitado el diseño de constructos moleculares basados en anticuerpos, que dirigen la eliminación de células infectadas, por medio de la actividad citotóxica de linfocitos T CD8+. Esto se logra debido a que un anticuerpo del constructo se une a la molécula CD3 presente en la membrana de todas las células T, mientras que el otro anticuerpo se acopla a las proteínas de la envoltura de partículas virales incipientes localizadas en la superficie de células infectadas. Esto evita el problema relacionado a la especificidad de los receptores de linfocitos citotóxicos para poder eliminar el virus. Estos estudios ofrecen un paso fundamental hacia la eliminación de reservorios virales latentes que persisten en pacientes en tratamiento antirretroviral.
Anticuerpos bi-específicos
El desarrollo de la terapia antirretroviral combinada para suprimir una infección por VIH y sus complicaciones ha sido un importante logro de la medicina moderna. Sin embargo, estos medicamentos no erradican el virus; sólo suprimen su ciclo de replicación celular. Este ciclo consiste en la integración del ADN viral en el genoma de la célula hospedera y la generación de nuevas partículas virales que se liberan por gemación. Pero una pequeña proporción de células sobrevive a las consecuencias líticas de la infección y forman un reservorio latente de células que poseen ADN viral integrado en los cromosomas celulares. Este depósito puede reactivar una abrupta infección si la terapia antirretroviral es interrumpida. Por este motivo, estrategias que erradiquen tales reservorios podrán lograr una cura completa y permitir que pacientes puedan descontinuar el costoso tratamiento, el que además posee efectos secundarios. Dos publicaciones proponen una mirada optimista: Julia A.M. Sung y equipo (J Clin Invest. 2015;125(11):4077–4090) y Amarendra Pegu y colaboradores (doi: 10.1038/ncomms9447), describen innovadores constructos moleculares diseñados para eliminar selectivamente estas células con infecciones latentes.
Para ser el blanco de fármacos, las células infectadas necesitan mostrar evidencia de que albergan el virus. Para las que sufren de una infección latente, esto requiere de la activación viral para reiniciar su ciclo replicativo. En los últimos años, los enfoques farmacológicos para la activación selectiva de estas células, se han basado en inhibidores de la histona desacetilasa, los que son diseñados para inducir la transcripción del ARN viral. Sin embargo, sólo una pequeña parte de las células responde a estos tratamientos. Además, la destrucción de las células activadas depende de la respuesta inmunitaria del paciente, pero esta ya se encuentra deteriorada y podría ser dirigida contra el virus infectivo inicial, el que puede haber mutado para evadir el reconocimiento inmunológico.
En los intentos de evitar estos problemas, ambos grupos de investigación, describen conceptualmente construcciones de proteínas similares, que combinan las especificidades de unión de dos anticuerpos diferentes (fig.1). Uno de los anticuerpos se une a un amplio espectro de proteínas de la envoltura viral, localizadas en la superficie de células infectadas de forma activa, típicamente linfocitos T CD4+ del sistema inmunológico; el otro, se une a la molécula CD3, que se expresa en la superficie de todos los linfocitos T. El fundamento de la técnica es dirigir el subconjunto células T CD8+, que tiene la capacidad de destrucción celular (citotoxicidad), de forma de eliminar las células con una infección latente, las que han sido inducidas para expresar proteínas de la envoltura viral. La participación de CD3 implica que cualquier célula T CD8+ puede dirigirse a las células infectadas, obviando la necesidad de que linfocitos T se unan específicamente a glicoproteínas de superficie del VIH (antígenos).
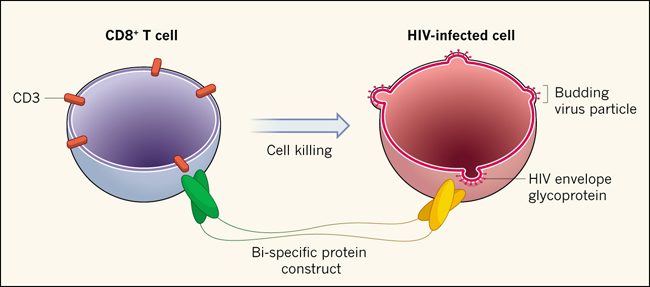
Figura 1: constructos bi-específicos
Sung y colegas y por otro lado Pegu y su equipo, presentaron dos construcciones diferentes de proteínas que combinan secciones de dos anticuerpos monoclonales: un anticuerpo se une a la molécula CD3 expresada en la superficie de todas las células T del sistema inmunitario, y el otro se une a proteínas de envoltura del VIH, que se expresan en la superficie de células infectadas. Estos constructos dirigen la eliminación directa de células infectadas, por parte de linfocitos CD8+ (citotóxicos), independientemente de si los receptores de estos linfocitos tienen especificidad para el virus. Esta orientación está diseñada para aumentar la eficacia de la respuesta inmunológica contra el VIH y ayudar a eliminar las poco comunes células con infección latente.
Ambos grupos mostraron que, in vitro, su construcciones funcionaban como se había propuesto, induciendo la eliminación directa de células que expresan proteínas de la envoltura viral, de forma independiente de la especificidad de antígeno de las células T CD8+. El constructo DART (por sus siglas en inglés, dual-affinity re-targetingre-targeting) descrito por Sung y colegas, también se probó ex vivo: se logró elmininar células provenientes de pacientes cuya infección fue bien suprimida con terapia antirretroviral, después de que las células habían sido inducidas para expresar proteínas de la envoltura (a través de la exposición a la proteína fitohemaglutinina o al inhibidor de histona desacetilasa, vorinostat). Por otro lado, Pegu y equipo demostraron que el brazo de unión de CD3 de su constructo no sólo activa la citotoxicidad de células T CD8+, sino que también sirve para activar linfocitos T CD4+ infectados de forma latente para que expresen proteínas de la envoltura del VIH, permitiendo su eliminación sin la inducción de otros factores. Sin embargo, serán necesarios estudios adicionales para proporcionar evidencia de la eliminación sustancial ex vivo de células de pacientes usando este constructo.
Muchas investigaciones anteriores han generado anticuerpos bi-específicos contra diversos objetivos, incluyendo antígenos de VIH y de células tumorales. Tales anticuerpos para combatir células infectadas por VIH, fueron descritos por primera vez en 1991, antes de que existieran las potentes terapias combinadas antiretrovirales y antes de que fuera concebible una cura contra el virus. Por otra parte, se ha demostrado que estos constructos de anticuerpos duales tienen la capacidad de eliminar células cancerosas en linfomas no Hodgkin. Sin embargo, la traducción de esta actividad in vitro a partir de un constructo molecular innovador hacia un tratamiento efectivo es un proceso desalentador.
Hay varias características biológicas que representan obstáculos para cualquier estrategia en la cura del VIH. Sólo una célula T CD4+ entre un millón, se infectan de forma latente, lo que significa que estas células son una diana poco común y difícil de detectar. Hasta el momento, no hay agentes identificados que induzcan la expresión de antígenos virales en la mayoría de las células con infección latente sin afectar a células sanas. Además, el reservorio latente puede incluir células en compartimientos anatómicos que los grandes constructos proteicos no pueden penetrar, tales como el sistema nervioso central y el tracto genital.
Adicionalmente, cada compuesto prometedor enfrenta un desarrollo sustancial de obstáculos antes de que pueda llegar a ser un fármaco eficaz. En primer lugar, la eficacia vista en modelos in vitro puede no ser replicada in vivo. Los medicamentos pueden mantenerse a una concentración constante en cultivo celular, pero esto es difícil de lograr in vivo, donde ocurre absorción, distribución y clearance del compuesto. En segundo lugar, la distribución de células diana y citotóxicas en tejidos, puede que no sea tan densa o uniforme en comparación a un cultivo celular. Una tercera consideración, es que ningún anticuerpo de unión a la envoltura se acoplará a todas las particulas virales de la superficie y por ende debe ser considerada la posibilidad de que alguna variante mutante del virus pueda escapar del reconocimiento mediada por el constructo.
Los efectos extra objetivo, también pueden ser una preocupación. El anticuerpo bi-específico de Pegu y colegas, indujo una rápida caída en el número de células que expresan CD3 en el torrente sanguíneo cuando fue infundido en macacos rhesus infectados, probablemente debido a la activación y la redistribución de las células. Además, el constructo también activa células T CD4+ no infectadas. En resumen, las proteínas del constructo pueden inducir respuestas inmunológicas en simios, como se documenta por los autores. En consecuencia, los anticuerpos anti-constructo generados durante estas respuestas podrían ser tóxicos, y pueden resultar en una disminución la actividad farmacológica.
La investigación de una cura para el VIH es un camino largo y difícil en sus etapas iniciales, por lo que todas las opciones innovadoras deberían ser bienvenidas e investigadas. Los anticuerpos monoclonales han logrado un éxito notable en el tratamiento de muchas condiciones, y las construcciones que aprovechen su especificidad para generar capacidades bifuncionales - tales como los presentados por los equipos de Sung y Pegu- son una de esas innovaciones dignas de mayor atención.
Fuente bibliográfica
HIV: Cure by killing
Douglas D. Richman.
Center for AIDS Research, University of California San Diego, La Jolla, California 92093-0679, USA.
doi:10.1038/nature16321