Señalización Notch y el melanoma maligno
Aumenta la evidencia que indica que la señalización de la proteína Notch contribuye a los procesos fisiológicos, incluyendo el desarrollo, la diferenciación y tumorigénesis, ya sea como un promotor o supresor tumoral, dependientes del contexto celular, nivel de expresión y la diafonía con otros sistemas de señalización. Además, a la vía Notch se le ha implicado en la regulación de la autorrenovación de células madre adultas y la diferenciación de precursores a lo largo de una línea celular específica en el normal desarrollo embrionario y la organogénesis. También existe información que la señalización a través de los receptores Notch regula la proliferación celular y la supervivencia celular en varios tipos de cáncer, incluyendo el melanoma maligno, con resultados opuestos dependiendo del tipo de tejido. La progresión tumoral/metástasis del melanoma maligno es un proceso complicado que requiere múltiples eventos celulares, incluyendo la proliferación celular, supervivencia, la migración e invasión.
La señalización de Notch parece ser un sistema prometedor para nuevas dianas terapéuticas en el tratamiento del melanoma, y tal vez en la prevención de su metástasis.
Notch, ARN y el melanoma
En los últimos años, un mejor conocimiento de la base molecular del melanoma ha podido modificar la atención de los pacientes. El melanoma metastásico es un ejemplo de los efectos que los descubrimientos científicos pueden tener en la clínica. Los avances en inmunología han dado a luz una nueva y poderosa clase de agentes asociados a la inmunoterapia, capaces de proporcionar un control estable de la enfermedad en una fracción importante de pacientes con melanoma. Para los tumores que no responden a la inmunoterapia, pero albergan mutaciones específicas en el oncogén BRAF (aproximadamente la mitad de todos los casos), la terapia con inhibidores farmacológicos de la proteína quinasa activada por mitógenos (MAPK) con efectores RAF y MEK ha demostrado ser muy beneficiosa (aunque sea transitoriamente). Ensayos clínicos en curso también hacen alusión positiva a la terapia dirigida en otros subtipos moleculares del melanoma. En un tipo de cáncer considerado como plaga incluso dentro de la oncología, los descubrimientos científicos con importancia clínica parecen ya casi un lugar común.
En este contexto, un reciente informe de Matteo Forloni y colegas (Elife 2014; 3: e01460) aportan sobre aspectos biológicos del melanoma, la genética y el desarrollo de fármacos. Estos investigadores trataron de estudiar los microARN (especies de ARN pequeños, intracelulares que regulan los niveles de ARN mensajeros específicos, pero no codifican proteínas) que se sobre-regulan cuando el gen oncogénico BRAF se expresa en las células. El microARN más expresado en este contexto, denominado miR-146a, resulta ser un blanco de la cascada de señalización MAPK – una vía que se hiperactiva a través del factor de transcripción MYC en respuesta a BRAF y a los oncogenes ANR relacionados – en muchos melanomas. Por otra parte, en varios ensayos experimentales se encontró una sobreexpresión forzada de miR-146a que promueve la tumorigénesis del melanoma.
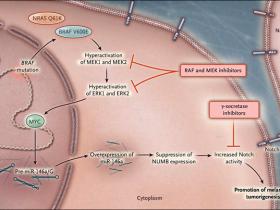
Esta especie de microARN es intrigante, ya que regula una vía independiente que puede ser susceptible de ser modulada por fármacos por derecho propio. En concreto, miR-146a suprime la expresión de NUMB, una proteína que regula negativamente a Notch, que es un receptor transmembrana que gobierna muchas funciones cruciales relacionadas con la comunicación célula-célula y la diferenciación celular (fig. 1). Al silenciar NUMB, la sobreexpresión de miR-146a aumenta la señalización de Notch en el melanoma. Este hallazgo se suma a una creciente evidencia que sugiere que Notch promueve el crecimiento de células tumorales en el melanoma.
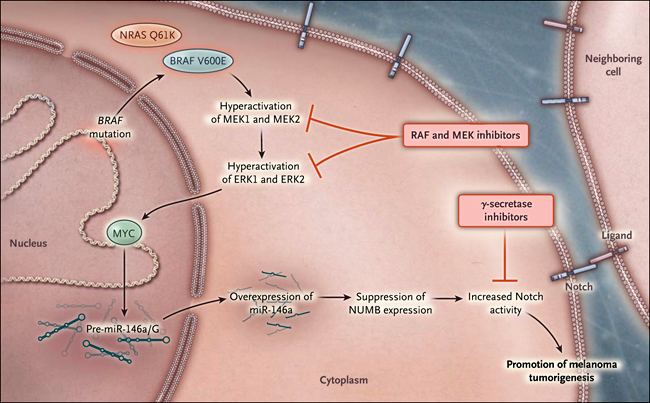
Figura 1: señalizaciones de BRAF, microARN y Notch en el melanoma.
Los autores descubrieron un microARN (miR-146a) que es sobre-expresado por la quinasa oncogénica MAP (MAPK) (por ejemplo, BRAF mutante o NRAS) y el factor de transcripción MYC en las células de melanoma. El precursor de miR-146a, en particular con su alelo G SNP, regula a la baja a NUMB, una proteína que suprime la actividad de Notch. Estos hallazgos sugieren que la señalización de Notch puede contribuir a la génesis del melanoma a través de la desregulación del microARN y que los inhibidores γ-secretasa, junto a los inhibidores de RAF y MEK, podrían ser considerados como una nueva combinación terapéutica a ser evaluado en ensayos clínicos.
Como miR-146a está regulado por las oncoproteínas BRAF y NRAS, los agentes terapéuticos dirigidos a la vía de Notch podrían, en teoría, ofrecer un beneficio clínico en el melanoma. Forloni y colegas proporcionan apoyo parcial a esta noción al probar una versión de NUMB que no puede ser suprimida por miR-146a: la expresión ectópica de NUMB mutante controla la regulación de Notch y deroga el crecimiento celular del melanoma. Por otra parte, los datos de ensayos clínicos generados por otros investigadores sugieren que los inhibidores de la γ-secretasa (fármacos que inhiben la señalización de Notch mediante la prevención de la escisión de su precursor) pueden producir importantes respuestas clínicas en el melanoma. Sin embargo, estas tentadoras evidencias deben ser consideradas a la luz del hecho de que Notch es sólo una de las variadas y posibles salidas oncogénicas de MAPK y que miR-146a no es el único regulador de la actividad de Notch en el melanoma.
Tal vez la observación más sorprendente surgida a partir del análisis del polimorfismo de un solo nucleótido en la secuencia pre-miR-146a fue la siguiente. El grupo de Forloni encontró que el ARN precursor de miR-146a con el alelo G exhibía un fenotipo tumorigénico y de silenciamiento de NUMB más robusto que su contraparte con el alelo C. Un estudio de nevos, de melanomas primarios y tumores metastásicos indicó que el alelo G estaba enriquecido durante la génesis y progresión del melanoma y que este enriquecimiento resulta en parte de una alteración somática C-a-G en este locus. Si este resultado se reproduce en estudios más amplios, podría ser una de las primeras manifestaciones de un mutación somática microRNA "conductura" muy recurrente en tumores sólidos en los seres humanos.
Por último, estos resultados invitan a la especulación que la adición de inhibidores de la γ-secretasa a los inhibidores de RAF y MEK puede ofrecer una mezcla terapéutica atractiva para la evaluación de futuros ensayos clínicos en el tratamiento del melanoma. Dada la toxicidad sustancial de los inhibidores de la γ-secretasa, sería beneficioso realizar estudios preclínicos adicionales de tales combinaciones en líneas celulares de melanoma y modelos de xenoinjertos derivados de pacientes. Tales ensayos podrían aclarar la generalización de la dependencia de Notch en el melanoma, la relevancia (si los hay) del alelo premiR146a G frente al alelo C para la estratificación del paciente, posibles dosis y el esquema de programación alternativa para reducir la toxicidad. En general, este estudio proporciona un recordatorio que, a pesar de los numerosos avances, recién se empieza a diseccionar la rica interacción entre los ARN no codificantes, la base biológica del cáncer y las potenciales estrategias terapéuticas.
Fuente bibliográfica
A Notch for Noncoding RNA in Melanoma
Levi A. Garraway, M.D., Ph.D.
Department of Medical Oncology, Dana–Farber Cancer Institute and Brigham and Women’s Hospital, Harvard Medical School, Boston; and the Broad Institute of Harvard and MIT, Cambridge, MA.
DOI: 10.1056/NEJMcibr1402173