Potencia regulatoria contra la autoinmunidad
Gracias al uso de nanopartículas revestidas con autoantígenos específicos aplicadas en modelos animales para el estudio de enfermedades autoinmunes e inflamatorias, se han logrado revertir complicaciones asociadas a procesos patológicos de diabetes tipo 1, encefalomielitis y artritis. Estos avances se reflejaron en la normalización glucémica, restauración de función motora y una resolución de la inflamación articular, para las enfermedades antes mencionadas. Todo lo anterior, involucra la intervención de linfocitos reguladores de tipo 1, células que recientemente han sido probadas como sustratos terapéuticos en la práctica clínica. Adicionalmente se está trabajando con modelos de ratones humanizados a partir de inyecciones de células mononucleares de pacientes diabéticos. El hallazgo más importante: la expansión de células T y B regulatorias, observación que representa una prometedora evidencia para el traspaso de este enfoque hacia terapias contra complicaciones autoinmunes en humanos.
Nanopartículas con autoantígenos
La tolerancia central es un proceso mediado en el timo y en la médula ósea, en el que células T y B autorreactivas, potencialmente patogénicas, se eliminan durante la ontogenia. Sin embargo, este proceso no es infalible: algunos cuerpos autorreactivos pueden escapar de esta selección. Nuevos agentes y mecanismos reguladores nuevos podrían mantener tales células bajo control. Entre estos, se encuentran las células T reguladoras (Treg), que son los blancos más prometedores para el tratamiento de patologías inflamatorias autoinmunes.
Entre los subconjuntos de células T reguladoras, aquellas que co expresan los marcadores CD4, CD25, y FOXP3 han sido los más estudiados. Estas células T FOXP3-positivas células, se seleccionan sobre la base de la auto-reactividad en el timo o sobre los niveles de inducción en tejidos periféricos, bajo la influencia de células presentadoras de antígenos (APC, por sus siglas en inglés) y citoquinas. Otro tipo relevante son las células T reguladoras de tipo 1 (Tr1), las que también se encuentran en la periferia. Las Tr1 expresan CD49b y LAG3, pero no FOXP3, y secretan las citoquinas antiinflamatorias interleuquina-10, 21, y el factor crecimiento transformante β (TGF- β).
Los linfocitos Tr1 han sido evaluados como sustratos terapéuticos en la clínica, pero al igual que su contraparte FOXP3 +, la preparación terapéutica contiene células T reguladoras específicas para múltiples antígenos. Hasta hace poco, se carecía de un método in vivo para expandir tales células específicas para un solo antígeno. Sin embargo, recientemente, Pere Santa Maria y colegas (Nature. 2016 Feb 25;530(7591):434-40) elaboraron un método donde participan las células Tr1, utilizando nanopartículas recubiertos con péptidos relevantes para enfermedades autoinmunes, unidos al complejo mayor de histocompatibilidad (MHC) de clase II (pMHCII-NP).
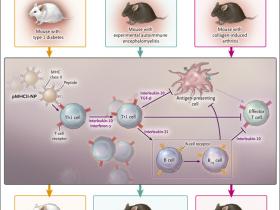
Actualmente es sabido que la presentación de antígenos por las APC en ausencia de la coestimulación mediada por moléculas B7-1 y B7-2 conduce a los linfocitos T al estado de anergia en la periferia. Sin embargo, los investigadores encontraron que la administración sistémica de pMHCII-NP restaura la normoglucemia en un modelo de ratón con diabetes tipo 1 autoinmune, y por otro lado, se observó una expansión de linfocitos T de memoria tipo Tr1 antígeno-específicos. Además, cuando utilizaron el mismo enfoque con pMHCII-NP que exhibe péptidos relevantes para complicaciones autoinmunes específicas como la encefalomielitis y artritis, evidenciaron efectos paliativos sobre los procesos patológicos usando el mismo modelo experimental in vivo. Específicamente, en la encefalomielitis autoinmune, encontraron que la expansión sistémica de células Tr1 se vincula con la restauración de la función motora, una activación reducida de la microglía y de macrófagos en el cerebelo, además de una disminución de la desmielinización de la medula espinal. Por otro lado, en el modelo de artritis en ratones, observaron una resolución de la inflamación articular (fig. 1). El efecto se mantuvo a pesar del predominio de otros autoantígenos e independientemente de si el antígeno estaba implicado en el inicio de la patología o en etapas posteriores. Los beneficios terapéuticos de las nanopartículas recubiertas con autoantígenos, mediados por los péptidos sobre pMHC II-NP, fueron específicos para la enfermedad, contribuyendo a la mejora de los órganos relevantes.
Sin embargo, ¿Cómo las pMHCII-NP amplian la población celular de Tr1 y cómo afectan estas células Tr1 las redes reguladoras? Los autores mostraron que estas células surgen a partir de células T helper de memoria que han tenido contacto con el antígeno, y que dependen de la presencia y secreción de interferón γ y de IL-10 (fig. 1). La presencia de la IL-10, TGF-β, y de -IL-21, pero no la de interferón-γ, es requerida por las células Tr1 para suprimir la enfermedad. Además, las células Tr1 potencian a linfocitos B reguladores productores de IL-10 mediante la secreción de IL-21. El efecto terapéutico de estas células B reguladoras se potencia de forma sinérgica con la expansión celular de las Tr1 promovida por pMHCII-NP.
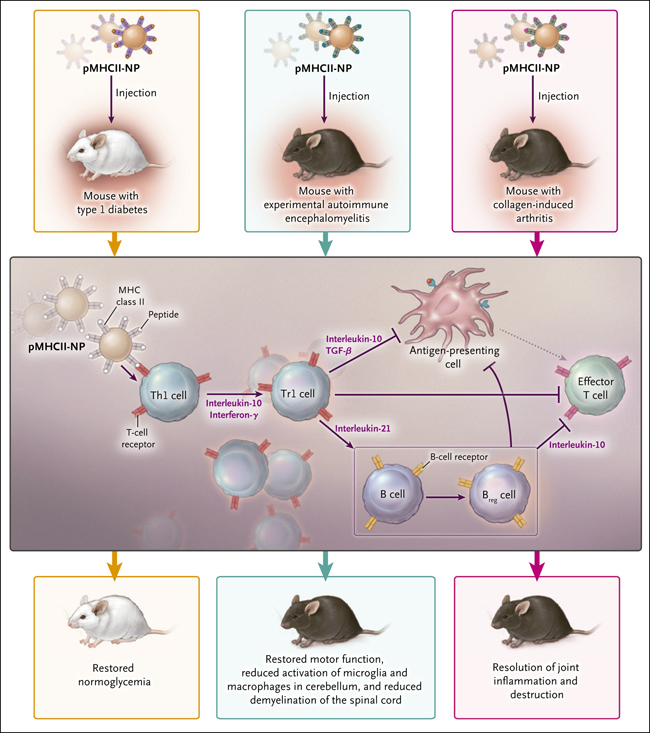
Figura 1. Regulación ejercida por células Tr1.
Las nanopartículas recubiertas con péptidos determinantes para enfermedades autoinmunes unidos al complejo mayor de histocompatibilidad (MHC) de clase II (pMHCII-NP) expanden la población de células T reguladoras de tipo 1 (células Tr1) específicas de antígeno en expermientos in vivo, y promueven beneficios terapéuticos en modelos de estudio para este tipo de patologías. Pere Santamaría y su equipo inyectaron el complejo pMHCII-NP en ratones con diabetes tipo 1, encefalomielitis autoinmune experimental, o con artritis inducida por colágeno. Encontraron que la administración sistémica de pMHCII-NP restablece la normoglucemia en ratones diabéticos, la función motora, reduce la activación de microglia y macrófagos en el cerebelo, y disminuye la desmielinización de la médula espinal en estos animales. Además promueve la resolución de la inflamación articular y su destrucción en ratones artríticos. Mecanísticamente, el complejo pMHCII-NP induce la generación y expansión de células Tr1 a partir de linfocitos T hepler tipo 1 (Th1) que ya han sido expuestas al antígeno, a través de un proceso dependiente de IL-10 e interferón-γ. Las células Tr1 potencian la proliferación de linfocitos B reguladores (Breg) productores de IL-10 de una manera dependiente de IL-21, lo cual tiene un efecto terapéutico positivo.
Adicionalmente, los investigadores demostraron que el complejo pMHCII-NP puede suprimir la autoinmunidad en modelos de ratón humanizado para diabetes tipo 1, que se generan mediante la inyección de células mononucleares de sangre periférica (PBMC, por sus siglas en inglés) obtenidas a partir de pacientes con inicio reciente de la complicación metabólica. Lo que encontraron en estos animales inmunosuprimidos con anterioridad, fue una proliferación de células tipo Tr1 y de células B regulatorias a partir de las PBMC humanas, observación que representa un paso inicial hacia la traducción de este enfoque a un tratamiento de enfermedades autoinmunes en seres humanos.
Aún con estos prometedores resultados, este estudio no es suficiente para cambiar el panorama terapéutico para las patologías de este tipo. Los hallazgos son de fase preclínica, pero a pesar de esto forman parte de un trabajo incipiente par traducir las investigaciones hacia avances clínicos. Actualmente, están siendo utilizados varios enfoques en la clínica dirigidos a células T reguladoras FOXP3 + y a linfocitos Tr1. Sin embargo, estas perspectivas apuntan a una población de linfocitos T reguladores policlonles, involucrando un tipo de inmunosupresión y por lo tanto podría darse una predisposición a infecciones y al cáncer. A pesar de esta preocupación, el complejo pMHCII-NP activa a células Tr1 de una forma antígeno-específica, lo cual permite disminuir la autoinmunidad patogénica sin comprometer sistémicamente el sistema inmunitario.
La seguridad a largo plazo es una preocupación de fondo, sobre todo porque un efecto duradero y protector probablemente dependerá de la exposición continua de células Tr1 al complejo pMHCII-NP. Además, se requiere de más investigación sobre la biodistribución y farmacocinética de estas nanopartículas. El uso de nanopartículas de óxido de hierro en la clínica, utilizadas con fines diagnósticos provee de un potencial soporte para la seguridad de esta parte del sistema. Tal fiabilidad dependerá de las futuras investigaciones clínicas que se realicen con el complejo pMHCII-NP, para poder determinar finalmente su uso como una terapia para las enfermedades autoinmunes.
Fuente bibliográfica
Repressing Immunity in Autoimmune Disease
Jagadeesh Bayry, D.V.M., Ph.D.
Institut National de la Santé et de la Recherche Médicale, Unité 1138, Centre de Recherche des Cordeliers, Paris.
DOI: 10.1056/NEJMcibr1602864